Зависимость скорости реакции от температуры. Правило Вант-Гоффа, особенности температурного коэффициента для биохимических процессов. Уравнение Аррениуса. Энергия активации
Скорость химической реакции зависит от многих факторов, среди которых находится температура. При повышении температуры увеличивается скорость движения молекул, возрастает число столкновений между ними и, соответственно этому доля активных молекул. Все это обусловливает увеличение скорости химических реакций с повышением температуры Количественно зависимость скорости гомогенных реакций от температуры может быть выражена установленным опытным путем в приближенной форме правилом Вант - Гоффа: при повышении температуры на каждые 10оС скорость гомогенной химической реакции увеличивается в 2-4 раза.
Уравнение, которое описывает это правило, следующее:
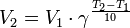
где  — скорость реакции при температуре
— скорость реакции при температуре  ,
, 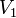 — скорость реакции при температуре
— скорость реакции при температуре 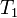 ,
,  — температурный коэффициент реакции, численно равен
— температурный коэффициент реакции, численно равен
отношению константы скорости при температуре Т + 10 к константе при температуре Т.
γ = k Т+10 / k Т.
Для большинства биохимических реакций температурный коэффициент Вант-Гоффа варьирует от 1,5 ¸ 3,0. Поэтому, если в результате какого-либо заболевания температура человеческого тела поднялась, например, с 36,50 до 39,50С, это значит увеличение скорости происходящих биохимических процессов в 1,13 – 1,39 раз, т.е. на 13-39%.
Объяснение зависимости скорости реакции от температуры было дано С.Аррениусом. К реакции приводит не каждое столкновение молекул реагентов, а только наиболее сильные столкновения. Лишь молекулы, обладающие избытком кинетической энергии, способны к химической реакции. С.Аррениус рассчитал долю активных (т.е. приводящих к реакции) соударений реагирующих частиц α, зависящую от температуры:
- α = exp(-E/RT)
и вывел уравнение Аррениуса для константы скорости реакции:
k = koe-Eа/RT,
где ko и Eа зависят от природы реагентов. Еа - это энергия, которую надо придать молекулам, чтобы они вступили во взаимодействие, называемая энергией активации. Она зависит от природы реагирующих веществ и является характеристикой любой реакции и обычно выражается в кДж/моль. Чем больше энергия активации, тем меньше активных молекул при данной температуре и тем медленнее идет реакция. Энергия активации быстро протекающих катализируемых реакций ниже, чем энергия активации соответствующих некатализируемых реакций. На этом основании часто говорят, что катализатор снижает энергию активации реакции.
Поясним на примере реакции в общем виде:
А2 + В2 = 2АВ
По оси ординат откладываем потенциальную энергию системы, а по оси абсцисс – ход реакции:
исходное состояние ---- переходное состояние – конечное состояние.

Чтобы войти в химический контакт друг с другом, реагирующие вещества А2 и В2 должны преодолеть энергетический барьер. На это затрачивается энергия активации. В случае применения катализатора значение энергии активации Еа меньше, чем без использования катализатора Еа/
Дата добавления: 2018-02-28; просмотров: 5755; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
