Теориялық негізі
Сұйықтарды кондуктометрлік әдіспен талдау сұйықтың меншікті электр өткізгіштігін өлшеуге негізделінген. Кондуктометрлік талдау әдісі үш түрлі әдістен тұрады. Атап айтса, олар мыналар: тура кондуктометрлік әдіс, кондуктометрлік титрлеу және хронокондуктометрлік титрлеу әдістері. Осылардың әрқайсысына аздап анықтама бере кетейік.
Тура кондуктометрлік әдісте анықталынатын электролиттің электр өткізгіштігін өлшеудің нәтижесінде оның концентрациясын анықталынады.
Кондуктометрлік титрлеу болса, сұйықтың концентрациясын титрлеу қисық сызығының сыну нүктесінің шамасына байланысты анықталынады.
Хронокондуктометрлік титрлеу әдісінде, сол сұйықты титрлеуге кеткен уақытқа байланысты анықталынатын заттың шамасын көрсеткіш өлшеу құралдарына жеткізеді.
Енді кондуктометрлік әдістің теориялық негізіне шолу жасайық..
Электр өткізгіштің өлшем бірлігі болып с и м е н с (См) қолданылады. Ол кедергіге қарама-қарсы шама. Электролит ерітіндісіндегі молекулалар оң және теріс иондарға ыдырайтыны белгілі. Оларды катиондар мен аниондар деп екіге бөледі.
Сұйықтың (электролиттің) электр өткізгіштігі төмендегі теңдіктің көмегімен анықталынады:
|
|
|
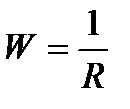 , (20.1)
, (20.1)
мұндағы W- сұйықтың электр өткізгіштігі; R - сұйықтың электр кедергісі,Ом. Ал, сұйықтың кедергісі болса, екі электродтың ара қашықтығына тура пропорционал да, олардың аудандарына кері пропорционал:
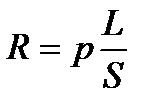 , (20.2)
, (20.2)
мұндағы L – екі электродтың ара қашықтығы, см; S – электродтың ауданы, см2. Коэффициент p (ом Ÿсм) сұйықтың меншікті кедергісі.
Сұйықтың электр өткізгіштігі болса, меншікті k және эквивалентті электр өткізгіштік болып екіге бөлінеді. Меншікті электр өткізгіштік пен сұйықтың меншікті кедергісінің арасындағы байланыс:
& 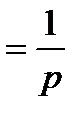 , (20.3)
, (20.3)
арқылы өрнектелінеді.
Егер С – элетролиттің концентрациясы (г-экв/л) болса, онда 1 см3 сұйықтың құрамында С/ 1000 г-экв/л болады. 1 г-экв ерітілген ерітіндінің көлемі (V, см3) 1000/ С тең. Сондықтан меншікті және эквивалентті электр өткізгіштердің арасындағы байланысқа біраз тоқтала кетейік.
Электролит ерітіндісінің электр өткізгіштігі әрбір иондардың электр өткізгіштігіне тәуелді. Иондардың электр өткізгіштігі болса, олардың эквивалентті электр өткізгіштігіне байланысты. Кез-келген ионның тұрақты токтың өрісіндегі қозғалу жылдамдығы оған әсер ететін күш Fi мен үйкелістің тұтқырлық күші Gi арқылы анықталынады:
|
|
|
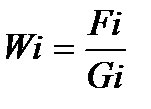 (20.4)
(20.4)
Егер Wi өрістің кернеулігіне Е бөлетін болсақ, онда 1 В/см кернеулігі бар өрістің ішіндегі ионның қозғалу жылдамдығы:
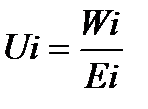 (20.5)
(20.5)
Ионның эквиваленттігі  оның қозғалу жылдамдығын
оның қозғалу жылдамдығын 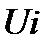 Фарадейдің санына
Фарадейдің санына 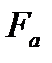 көбейткенге тең:
көбейткенге тең:
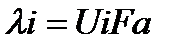 (20.6)
(20.6)
Молярлы өткізгіштік дегеніміз аниондар мен катиондардың эквиваленттіктерінің қосындысына тең, яғни:
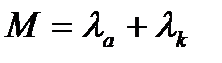 (20.7)
(20.7)
Осы аниондар мен катиондардың өзара бір-бірімен әсерлесуінің нәтижесінде иондардың эквиваленттіліктері 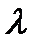 , сонымен қатар, олардың молярлы өткізгіштіктері М сұйықтың концентрациясына тәуелді болып келеді.
, сонымен қатар, олардың молярлы өткізгіштіктері М сұйықтың концентрациясына тәуелді болып келеді.
Дебай мен Хюккельдің күшті электролиттерге арналған теориясының көмегімен [14,15] концентрациясы С сәйкес болатын молярлы өткізгіштікті Мс, концентрациясы нөлге тең сұйықтың молярлы өткізгіштігі М0 арқылы өрнектеп табуға болады:
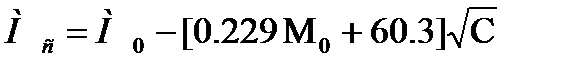 (20.8)
(20.8)
Өлшеу құалдарының көмегімен анықтауға болатын сұйықтың меншікті өткізгіштігі & мен молярлы өткізгіштік Мөс арасындағы байланыс төмендегі теңдік арқылы өрнектелінеді:
|
|
|
&=C Мс/1000. (20.9)
Дата добавления: 2015-12-21; просмотров: 1; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
