IV . Виведення молекулярної формули за об’ємом кисню, необхідного для спалювання органічної речовини
Приклад
На спалення 0,5 моль етиленового вуглеводню витрачається 33,6 л кисню (н.у.). Встановити формулу сполуки.
 Дано: Розв’язування:
Дано: Розв’язування:
υ(СnH2n) = 0,5 моль 1. Знаходимо кількість кисню:
 V(O2) = 33,6 л
V(O2) = 33,6 л 
СnH2n - ? 2. Складаємо рівняння реакції горіння етиленового вуглеводню у загальному
вигляді і розставляємо коефіцієнти:
СnH2n + хO2 → nСО2 + nН2О
n+2n=2x
3n=2x

3.Складаємо пропорцію:
На 1 моль СnH2n йде 1,5 моль O2 (n)
На 0,5 моль СnH2n йде 1,5 моль О2 (за умовою)

Отже , у молекул і етиленового вуглеводню два атоми Карбону. А на два атоми Карбону припадає
чотири атоми Гідрогену. Формула вуглеводню С2Н4, це етилен.
Відповідь: формула вуглеводню С2Н4 (етилен)
V . Виведення молекулярної формули за об’ємними відношеннями газів
Приклад
При дегідратації первинного насиченого спирту утворився газоподібний алкен, об’єм якого виявився в 4 рази меншим, ніж об’єм карбон(VI)оксиду, що утворився при спалювані такої ж кількості спирту. Одержаний алкен може повністю знебарвити розчин бромованої води, де міститься 16г брому. Який спирт піддали дегідратації?
Дано: Розв’язування:
 Складаємо рівняння відповідних реакцій:
Складаємо рівняння відповідних реакцій:
 m(Br2) = 16г 1) Дегідратація первинного насиченого спирту:
m(Br2) = 16г 1) Дегідратація первинного насиченого спирту:
|
|
|

 СnH2n+1OH - ? СnH2n+1OH СnH2n + H2O
СnH2n+1OH - ? СnH2n+1OH СnH2n + H2O
2) Горіння первинного насиченого спирту:
 СnH2n+1OH + О2 СО2 + Н2О
СnH2n+1OH + О2 СО2 + Н2О
3) Приєднання брому алкеном:
 СnH2n + Br2 СnH2n Br2
СnH2n + Br2 СnH2n Br2
Складаємо співвідношення реагуючих речовин та продуктів реакції:
V(СnH2n) : V (CO2) = 1:4
4) Знаходимо к іл ьк і сть речовини Брому :
 , за рівнянням υ(СnH2n) = 0,1 моль
, за рівнянням υ(СnH2n) = 0,1 моль
5) За умовою задачі:
 1V СnH2n 4V CO2
1V СnH2n 4V CO2
υ(СnH2n) = 0,1 моль
υ(CO2) = 0,4 моль
υ(СnH2n): υ(CO2) = 0,1 : 0,4 = 1:4
6) Формула алкену містить 4 атоми Карбону:
С4Н8
При гідратації алкену добудемо одноатомний насичений спирт С4Н9ОН
Відповідь: С4Н9ОН – бутанол
V І. Виведення молекулярної формули за рівнянням стану ідеальних газів
Приклад
 У сталеву посудину, місткість якої 2,75л, помістили 1,32г насиченого одноатомного спирту. Потім туди ввели 3,36л кисню (н. у.). Після підпалювання спирт повністю згорів, при цьому тиск у посудині за температурою 227ºС становив 306 кПа. Визначте формулу спирту.
У сталеву посудину, місткість якої 2,75л, помістили 1,32г насиченого одноатомного спирту. Потім туди ввели 3,36л кисню (н. у.). Після підпалювання спирт повністю згорів, при цьому тиск у посудині за температурою 227ºС становив 306 кПа. Визначте формулу спирту.
Дано: Розв'язування :
Vпосуду = 2,75л 1) За рівнянням Менделєєва-Клапейрона:
m(CnH2n+1OH) = 1,32г 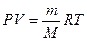
V(O2) = 3,36л Виводимо формулу для визначення кількості речовини суміші продуктів
|
|
|
T = 227ºС згорання:
 P =306 кПа
P =306 кПа  , Т = 227 + 273 = 500 К;
, Т = 227 + 273 = 500 К;
CnH2n+1OH - ? R = 8,314 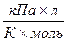

2) За законом збереження маси речовини, знаходимо масу кисню витраченого для спалювання насиченого одноатомного спирту:


3) Маса вихідних речовин:

Маса продуктів реакції:

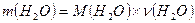
Приймаємо υ(СО2) = х,
υ(Н2О) = 0,2025-х
Складаємо математичне рівняння за законом збереження мас речовин:
6,12 = 44х + (0,2025-х)18
6,12 = 44х + 3,645 – 18х
2,475 = 26х
х = 0,095
Отже, υ(СО2) =0,095 моль, υ(Н2О) = 0,1075 моль
4) Складаємо рівняння реакції горіння насиченого одноатомного спирту:
 CnH2n+1OH + О2 5СО2 + 6Н2О
CnH2n+1OH + О2 5СО2 + 6Н2О
За співвідношенням υ(СО2) : υ(Н2О) = 0,095:0,1075 = 5:6
В сполуці спирту 5 атомів Карбону і 12 атомів Гідрогену.
Отже формула насиченого одноатомного спирту С5Н11ОН
Відповідь: С5Н11ОН – пентанол (аміловий спирт)
Дата добавления: 2022-11-11; просмотров: 28; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
