Эксперименты Высоцкого и Корниловой.
О ТРАНСМУТАЦИИ СТАБИЛЬНЫХ ИЗОТОПОВ
В ЖИВЫХ ОРГАНИЗМАХ
Ортодоксальная наука полагает, что в живых организмах происходят лишь химические превращения вещества, не затрагивающие атомных ядер. Эта доктрина возникла не на пустом месте. Опыт, полученный при попытках осуществления превращений нуклидов в результате искусственных ядерных реакций, показал, что продукты этих превращений радиоактивны, а сами эти превращения имеют высокие энергетические пороги и сопровождаются выделением большого количества энергии. Отсюда и возникла твёрдая убеждённость в том, что если в живых организмах происходила бы трансмутация элементов, то она была бы для этих организмов самоубийственна.
По логике такого подхода, живые организмы, для построения своих тел и обеспечения процессов жизнедеятельности в них, вынуждены довольствоваться атомами только тех элементов, которые они могут позаимствовать извне, из окружающей среды. Соответственно, организм способен выделить из себя только те атомы, которые он ранее позаимствовал. Факты, которые не укладываются в эти нехитрые правила, до сих пор игнорируются официальной наукой.
Между тем, известны не только косвенные свидетельства о превращениях элементов в живых организмах, давно подмеченные животноводами и растениеводами (см., например, популярные обзоры [1,2]). Известны не только наивные и уязвимые для критики попытки доказательств таких превращений. Ещё известны эксперименты [3], выполненные, по современным меркам, на высочайшем техническом и методологическом уровне – и их результаты, с применением современных методов элементного и изотопного анализов, с полной определённостью указывают на то, что ядерные превращения в биологических объектах имеют место. При этом биотрансмутация не порождает радиоактивных излучений и, в отличие от свободной трансмутации при экстремальных воздействиях на вещество, биотрансмутация не сопровождается аномальным энерговыделением.
|
|
|
Эти особенности биотрансмутации – как и сам её факт – совершенно не укладываются в рамки традиционных подходов, поэтому предложенные на сегодня модели физического механизма биотрансмутации едва ли можно считать адекватными. В рамках же представлений о «цифровом» физическом мире рассматривается концепция поведения вещества в одушевлённых организмах, рассмотрение которой выходит за рамки настоящей статьи.
Косвенные свидетельства и ранние эксперименты.
Приведём результаты некоторых опытов (из обзора [4]).
Косвенным свидетельством о трансмутации в проростках растений может служить увеличение в них содержания тех элементов, которые не могли быть получены в таких количествах с водой и воздухом.
|
|
|
Вогель (1844 г.) выращивал ростки на неорганическом субстрате (толчёном стекле) и обнаружил в них увеличение количества серы.
Герцель с 1875 по 1883 гг. выполнил ряд исследований с прорастающими семенами разных растений. Обнаружились изменения содержания кальция, калия и фосфора при прорастании. Добавление в воду солей кальция увеличивало в семенах производство калия. Добавление K 2 CO 3 увеличивало производство кальция.
Баранже с 1950 по 1970 гг. тоже экспериментировал с прорастающими семенами. Анализировалось содержание фосфора, калия, кальция и железа. Прорастание выполнялось в контролируемой среде, при поливе водой двойной дистилляции. Обнаружилось увеличение количеств Ca на 4.2%, Fe – на 8.3%, а также уменьшение количеств P на 1.9% и K на 1.1%. Добавление в воду MnCl 2 увеличивало выход железа. Была набрана богатая статистика; никто не нашёл ошибок и не оспорил результаты.
Кервран (1960-1980 гг.) обратил внимание на то, что рабочие-нефтяники Сахары ежедневно выделяют с экскрементами, в среднем, по 320 mg Ca больше, чем они получают его с пищей, водой и воздухом – при этом нет каких-либо признаков декальцинирования организма. Заметил, что куры в тех областях Британии, где почвы крайне бедны кальцием, ежедневно несут яйца с нормальной скорлупой, содержащей Ca – опять же, без признаков декальцинирования организма. Эти куры охотно заглатывают кусочки слюды, содержащей калий. Был сделан вывод: куры превращают часть K в Ca (кстати, замечено: если кормить кур пищей, бедной и кальцием, и калием, то они несут яйца с мягкой скорлупой; но если начать давать им пищу, бедную кальцием и богатую калием, то скорлупа их яиц быстро приходит в норму, в ней кальция становится столько, сколько нужно). Также экспериментировал с прорастающими семенами и нашёл, что количества K и Ca в них изменяются, причём, потеря массы K и прирост массы Ca, практически, равны по величине.
|
|
|
Комаки (1970-1980 гг.) показал, что восемь штаммов микроорганизмов, выращенных на культурах с дефицитом калия, увеличили его содержание через превращение Ca ® K.
Энгель и Грубер (2006) проращивали маш на растворе MnCl 2. Они обнаружили прирост количества железа. Предположили, что происходит реакция Mn 55 + H 1 ® Fe 56 .
К чести автора обзора [3], он привёл и отрицательные результаты – тех опытов, в которых биотрансмутация не обнаружилась. Но эти опыты, на наш взгляд, ничуть не бросают тень на обнаруженные факты биотрансмутации. Не будем забывать о том, что речь идёт о превращениях вещества, происходящих в живом организме – а, значит, происходящих тогда, когда соблюдён ряд предусловий, причём, не все эти предусловия нам известны.
|
|
|
Эксперименты Высоцкого и Корниловой.
Отдельно следует сказать про эксперименты Высоцкого и Корниловой [3] – которые, на сегодня, обладают, по-видимому, наивысшей доказательной силой. Эти авторы не пассивно исследовали происходящее в биологических системах, а сами создавали условия, подталкивающие биологическую систему к осуществлению реакций трансмутации, желаемых экспериментаторами и выбираемых из соображений высоко-селективной и надёжной идентификации продуктов трансмутации. Такими продуктами считаются, например, изотопы железа. Они идентифицировались двумя методами: с помощью мёссбауэровской спектроскопии и лазерной масс-спектрометрии. В качестве подопытных биологических объектов, которых стимулировали производить биотрансмутацию, использовались определённые виды бактерий и дрожжей – ввиду быстроты их размножения и удобства проведения элементного и изотопного анализов выращенной культуры.
Авторы ожидали, что в культуре, растущей в дефицитной по железу питательной среде на основе тяжёлой воды с добавлением солей марганца, будет осуществляться превращение марганца в железо через присоединение дейтрона: Mn 55 + d 2 ® Fe 57. Изотоп железа Fe 57 надёжно идентифицируется методом мёссбауэровской спектроскопии, а, поскольку его природное содержание мало, то его накопление уверенно выявляется через масс-спектроскопическое определение соотношения количеств изотопов железа в выращенной культуре.
В исходном материале наличие изотопа Fe 57 не обнаруживалось – как и в культурах, выращенных в средах, неоптимальных для ожидаемой реакции. Но мёссбауэровская спектральная линия, соответствующая этому изотопу, уверенно обнаруживалась в культурах, выращенных в оптимальных средах. Коэффициент трансмутации составил для дрожжевой культуры (1.90±0.52)×10-8 ядер Fe 57 на одно ядро Mn 55 за одну секунду, а для культуры бактерий Deinococcus Radiodurans – (1.30±0.46)×10-8 ядер Fe 57 на одно ядро Mn 55 за одну секунду. Анализ же с помощью лазерной масс-спектрометрии показал, что в культурах, выращенных в неоптимальных средах, отношения содержания изотопов Fe 57 и Fe 56 равны своему природному значению, а именно, h(Fe 57)/h(Fe 56)»0.02, тогда как в культурах, выращенных в оптимальных средах, это соотношение превышает природное значение в 35-40 раз: h(Fe 57)/h(Fe 56)=0.7-0.9. При этом коэффициент трансмутации, определённый с помощью масс-спектрометрии, примерно совпал со значением, полученным с помощью мёссбауэровской спектроскопии.
Кроме того, авторы [3] полагали, что в культуре, растущей в дефицитной по железу среде, дополненной контролируемыми количествами одноизотопных элементов Na 23 и P 31, будет происходить реакция Na 23 + P 31 ® Fe 54. При том, что природное соотношение изотопов Fe 54 и Fe 56 составляет h(Fe 54)/h(Fe 56)»0.06, их соотношение в культурах, выращенных в оптимальных средах, составило h(Fe 54)/h(Fe 56)=0.20-0.25. Коэффициенты трансмутации составили: по фосфору – (3-6)×10-10 ядер Fe 54 на одно ядро P 31 за одну секунду, а по натрию – (1-2)×10-10 ядер Fe 54 на одно ядро Na 23 за одну секунду. Также обнаружилось, что добавление в питательную среду солей цезия приводило к существенному увеличению продуцирования изотопа Fe 54, что давало в выращенной культуре соотношение h(Fe 54)/h(Fe 56)=1.0-1.5.
Попутно, авторам [3] удалось установить факт превращения цезия в барий: Cs 133 + p 1 ® Ba 134, с коэффициентом трансмутации »10-8 ядер Ba 134 на одно ядро Cs 133 за одну секунду. Этот результат они считают первым успешным обнаружением биотрансмутации тяжёлых элементов.
Перечисленные результаты Высоцкого и Корниловой имеют, на наш взгляд, огромное значение – поскольку, в их методике, обнаруживаемые изотопы не могли иметь иное происхождение, кроме как быть продуктами биотрансмутации. Вместе с тем, вопрос о том, какими, в действительности, путями образовывались эти продукты биотрансмутации, не может считаться окончательно решённым. Кроме того, авторы умалчивают о том, что поведение вещества в живых организмах очень сильно отличается от его поведения в неодушевлённых предметах. Соответственно, они не объясняют, почему реакции трансмутации, о которых они ведут речь, могут происходить только в биологических системах.
Ниже мы изложим некоторые соображения по этим вопросам.
Дорожка стабильных изотопов.
Хорошо известно, что в стабильных нуклидах, по мере увеличения атомного номера, число нейтронов становится всё больше, чем число протонов. Отсюда, будто бы, следует, что для превращения исходного стабильного нуклида в стабильный же нуклид с атомным номером, большим на единицу, требуется добавить в исходный нуклид не просто протон, и не просто протон и нейтрон (ядро дейтерия) – а, возможно, протон и два нейтрона (ядро трития, которое не только является редкостью, но ещё и нестабильно). В действительности же, такие превращения – с изменением атомного номера на единицу – отнюдь не требуют обязательного задействования ядер дейтерия и, тем более, ядер трития.
На Рис.1,2 изображена дорожка стабильных изотопов, от бериллия 4 Be 9 до висмута 83 Bi 209, (чтобы не загромождать схему, некоторые редкие изотопы не показаны). Дорожка разбита на пять частей; для каждой из них указана своя система координат, в которой по оси абсцисс отложены количества протонов (P) в ядрах и, соответственно, атомные номера изотопов, а по оси ординат – количества нейтронов (N) в ядрах.
Хорошо видно, что, практически, весь диапазон элементов от 4 Be до 83 Bi заполняют пары стабильных нуклидов, которые имеют различающиеся на единицу атомные номера и одинаковые количества нейтронов. В этом диапазоне, лишь два элемента не имеют стабильных изотопов – технеций 43 Tc и прометий 61 Pm. Для технеция мы указали три изотопа с периодами полураспада ~105-106 лет – что, при сопоставлении с характерными временами изменений в живых организмах, можно трактовать как полную стабильность. Более слабым звеном в дорожке стабильных изотопов является элемент прометий, изотоп которого 61 Pm 146, допускающий однопротонное превращение в стабильный изотоп самария 62 Sm 147, имеет период полураспада в 4.4 года – но, для случая одноклеточных организмов, этот изотоп тоже можно считать стабильным.

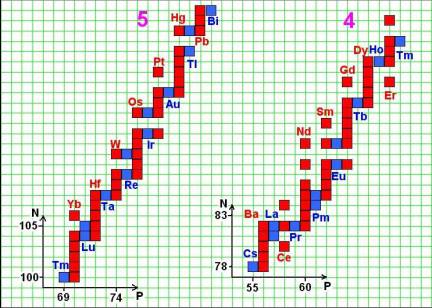
Рис.1, Рис.2. Дорожка стабильных изотопов от бериллия до висмута.
Красным цветом показаны элементы с чётным количеством протонов,
синим – с нечётным количеством протонов.
Наличие пар стабильных изотопов соседних элементов, имеющих одинаковые количества нейтронов, подсказывает нам, что, при управляемой трансмутации стабильных изотопов в живых организмах, процедуры изменения количества протонов и количества нейтронов в ядре могут выполняться независимо друг от друга. Т.е., каждое элементарное продвижение по дорожке стабильных изотопов представляет собой либо шаг вправо-влево (изменение P), либо шаг вверх-вниз (изменение N). Как можно видеть, для шага вверх или вниз требуется, в некоторых случаях, добавлять или удалять два нейтрона. Но, даже с учётом этих случаев, стратегия, при которой количества протонов и нейтронов управляемо изменяются по отдельности, гораздо проще в реализации, чем стратегия присоединения-отделения нуклонных комплексов, включающих в себя как протоны, так и нейтроны.
Но дело не только в простоте реализации той или иной стратегии. Слияние двух стабильных составных нуклидов даёт нуклид, который оказывается, как правило, с недостатком нейтронов, т.е. является нестабильным. А составные ядра, которые являются продуктами расщепления стабильного нуклида, имеют, как правило, избытки нейтронов – т.е., они, опять же, являются нестабильными. Стратегия же последовательных минимальных изменений либо только количества нейтронов, либо только количества протонов в нуклиде – гарантирует стабильность продуктов трансмутации. Вот почему трансмутации стабильных изотопов в живых организмах, при которых атомный номер изменяется всего на единицу, представляются нам наиболее вероятными.
Действительно, как отмечалось выше, имеются указания на то, что в живых организмах происходят взаимные превращения стабильных изотопов соседних элементов – например, в таких парах, как Na 23 и Mg 24, P 31 и S 32, K 39 и Ca 40, Mn 55 и Fe 56. Заметим, что все названные изотопы в этих четырёх парах являются, для своих элементов, самыми распространёнными – едва ли это можно списать на простые совпадения.
1. https://www.kramola.info/vesti/neobyknovennoe/biologicheskaya-transmutaciya-ili-otkuda-v-yaycah-kalciy
2. http://alchemy.ucoz.ru/publ/naturalnye_alkhimiki/2-1-0-40
3. В.И Высоцкий, А.А.Корнилова. Ядерный синтез и трансмутация изотопов в биологических системах. М., "Мир", 2003.
4. Jean-Paul Biberian. Biological Transmutations: Historical Perspective. J. Condensed Matter Nucl.Sci., 7 (2012) 11-25.
5. Таблицы физических величин. Справочник. Под ред. акад. И.К.Кикоина. М., «Атомиздат», 1976.
Дата добавления: 2022-06-11; просмотров: 40; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
