Определение фотохимической реакции
Фотохимическими называют химические реакции, протекающие под воздействием облучения реакционной смеси видимым или ультрафиолетовым светом (  , фотолиз).
, фотолиз).
Действие света заключается в том, что молекулы реагентов, поглощая свет переходят в возбужденное энергетическое состояние и потому обладают повышенной реакционной способностью.
Стадии фотохимической реакции.
1. Фотохимическая реакция - многостадийный физикохимический процесс, в котором, обычно, выделяют 2 основных этапа:
а) Первичный фотохимический процесс - процесс, к которому относят акт поглощения кванта света с непосредственно сопровождающими его физико-химическими процессами.
б) Вторичные химические реакции – реакции, которые не требуют для своего протекания электромагнитного облучения, но являющиеся следствием этого облучения.
2. Первичный фотохимический процесс (выделяют 2 стадии):
а) Начальный акт поглощения - взаимодействие молекулы с квантом света, в результате которого она переходит в электронно-возбужденное состояние: 
б) Первичные фотохимические превращения
1) химические – взаимодействие с другими молекулами

внутримолекулярные превращения 
фотодиссоциация на атомы или радикалы
 и др.
и др.
2) физические – дезактивация при столкновении со стенкой
|
|
|
или нейтральной молекулой
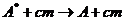 ,
, 

флуоресценция  и др.
и др.
3. Вторичные (темновые) процессы
а) продукты первичных превращений – нейтральные молекулы
б) – активные частицы (атомы или радикалы)
а) 
б) 
 и т.д.
и т.д.
Основные законы фотохимии.
1. Закон Гротгуса-Дрепера.
Только поглощаемое средой излучение способно вызвать в ней химическое изменение.
2. Закон Штарка-Энштейна (1912г.)
Каждый поглощенный квант света способен в первичном фотохимическом акте активизировать только одну молекулу, т.е. вызвать химическое превращение одной молекулы.
3. Закон Ламберта-Беера, 

Квантовый выход фотохимической реакции.
1. Полный квантовый выход
а) Квантовый выход – отношение числа прореагировавших молекул к числу поглощенных квантов света.



б) Пределы изменения квантового выхода.
1) 
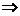 выполняется закон Эйнштейна
выполняется закон Эйнштейна
2) 
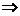 физическая дезактивация, отсутствие вторичных процессов (низкие
физическая дезактивация, отсутствие вторичных процессов (низкие  )
)
3) 
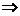 а)
а)  ,
, 

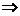

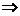


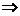 б) цепной механизм реакции
б) цепной механизм реакции
2. Квантовый выход первичной фотохимической реакции.
|
|
|
- отношение числа прореагировавших возбужденных молекул в акте первичного фотохимического превращения к числу поглощенных квантов света  .
.
Кинетика фотохимической реакции
1. Скорость реакции, 




2. Закон Ламберта-Беера, 


3.  ,
, 
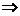



а) 
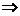
 ,
, 
б) 
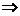
 ,
, 
Сенсибилизированные фотохимические реакции.
1. Сенсибилизация – придание несветочувствительным веществам способности к фотохимическим превращениям.
2. Сенсибилизаторы – вещества, которые непосредственного участия в химическом процессе не принимают, но поглощают кванты света и передают проглощенную энергию реагентам, которые и испытывают затем химическое превращение.
3. Пример: фотохим. разложение  в присутствии паров
в присутствии паров  .
.
а) 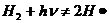
б) 

Дата добавления: 2018-02-18; просмотров: 1683; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
