Расчёт значений средних теплоёмкостей
Рассчитать значение средней удельной теплоёмкости в некотором заданном интервале температур от t1 до t2 оС можно как по таблицам средних теплоёмкостей, так и по эмпирической формуле для истинной теплоёмкости.
Расчёт по таблицам ведётся на базе формулы определения средней теплоёмкости (9.2):
 , (9)
, (9)
где  – средняя удельная теплоемкость в интервале температур от t1 до t2, Дж/(кг · К).
– средняя удельная теплоемкость в интервале температур от t1 до t2, Дж/(кг · К).
При этом значение теплоты q, которую необходимо подвести к 1 кг вещества чтобы нагреть его от t1 до t2 оС, определяется как разность двух теплот: теплоты  , которая затрачивается на нагрев от 0 до t2 оС и теплоты
, которая затрачивается на нагрев от 0 до t2 оС и теплоты  , которая затрачивается на нагрев от 0 до t1 оС:
, которая затрачивается на нагрев от 0 до t1 оС:
 , Дж/кг. (10)
, Дж/кг. (10)
Для вычисления  и
и  в таблицах выбираем значение средней теплоёмкости при температуре t2 – это средняя теплоёмкость в интервале температур от 0 до t2 оС:
в таблицах выбираем значение средней теплоёмкости при температуре t2 – это средняя теплоёмкость в интервале температур от 0 до t2 оС:  .
.
Соответственно будем иметь:
 . (11)
. (11)
Аналогичным образом получаем:
 , (12)
, (12)
где  – табличные данные средней теплоёмкости при температуре t1, Дж/(кг · К).
– табличные данные средней теплоёмкости при температуре t1, Дж/(кг · К).
После подстановки (11) и (12) в (9) окончательно получаем формулу:
 . (13)
. (13)
По формуле для истинной теплоёмкости значение средней теплоёмкости в интервале температур от t1 до t2 определяется как среднеинтегральное от функции с(t) в данном интервале температур.
Пусть эмпирическая формула для истинной удельной теплоёмкости имеет вид, аналогичный (9.2):
|
|
|
с(Т) = a1 + a2 · t + a3 · t –2, (14)
где t – температура, oC; a1, a2 и a3 – известные для конкретного вещества коэффициенты.
Тогда формула для вычисления средней теплоёмкости в интервале температур от t1 до t2 имеет вид:
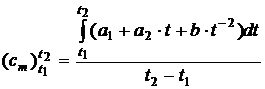 . (15)
. (15)
Теплоёмкость смеси идеальных газов
Рассмотрим идеальную газовую смесь, состоящую из n компонентов, масса которой М, кг. Для наглядности будем считать, что смесь нагревается в интервале температур равном одному градусу. Для нагрева такой смеси на один градус Цельсия (или Кельвина) необходимо температуру каждого из компонентов повысить на один градус.
Следовательно, к каждому компоненту необходимо подвести теплоту Qi, которая повысит температуру этого i-го компонента на один градус:
Qi = mi · ci · 1, Дж, (16)
где mi – масса i-го компонента, кг; ci – удельная массовая теплоёмкость i-го компонента, Дж/(кг · К).
Очевидно, что количество теплоты, необходимое для нагрева всей смеси на один градус Qсм, равно сумме теплот, необходимых для нагрева каждого компонента:
 , Дж. (17)
, Дж. (17)
С другой стороны по определению удельной массовой теплоёмкости смеси ссм имеем:
|
|
|
Qсм = М · ссм · 1, Дж. (18)
Исходя из (17) и (18) можем записать:
 . (19)
. (19)
После деления обоих частей (19) на М получаем формулу для расчёта удельной массовой теплоёмкости смеси:
 , Дж/(кг · К), (20)
, Дж/(кг · К), (20)
где gi – массовая доля компонента, кг/кг.
Так как химический состав смеси всегда задан, то значения массовых долей компонентов gi известны и по формуле (20) всегда можно рассчитать ссм.
Повторив рассуждения для объёмных и мольных удельных теплоёмкостей, можно легко получить аналогичные формулы:
с΄см =  , (21)
, (21)
μссм =  , (22)
, (22)
где  и μссм – удельные объёмная и мольная теплоёмкость смеси соответственно, Дж/(нм3 · К), Дж/(моль · К); ri – объемная доля i-го компонента смеси; ki – мольная доля i-го компонента смеси; c'i и μci – удельные объёмная и мольная теплоемкость i-го компонента смеси, Дж/(нм3 · К), Дж/(моль · К).
и μссм – удельные объёмная и мольная теплоёмкость смеси соответственно, Дж/(нм3 · К), Дж/(моль · К); ri – объемная доля i-го компонента смеси; ki – мольная доля i-го компонента смеси; c'i и μci – удельные объёмная и мольная теплоемкость i-го компонента смеси, Дж/(нм3 · К), Дж/(моль · К).
В формулах (21) и (22) следует учитывать, что объёмные доли численно равны мольным долям ri = ki (см. п. 3.2. Приложения 3).
Таким образом при заданном химическом составе смеси значения ri известны и по формулам (21) и (22) всегда можно рассчитать  и μссм.
и μссм.
|
|
|
Следует отметить, что по формулам (20) – (22) могут быть рассчитаны средние и истинные теплоёмкости как при постоянном давлении, так и при постоянном объёме.
Приложение 6
Дата добавления: 2018-02-15; просмотров: 8054; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
