Численное решение радиальных задач
В данной работе с помощью персонального компьютера производится численное решение стационарного уравнения Шредингера одномерной радиальной задачи (6.15), которое можно записать в виде:
 , ,
|
причем конкретное выражение для эффективной потенциальной функции зависит от орбитального квантового числа. Следовательно, каждому значению орбитального квантового числа соответствует отдельное уравнение т. е. своя задача. В работе решаются s-, p- и d-задачи, для которых значения орбитального квантового числа равны 0, 1, и 2.
Радиальную координату удобно выражать в ангстремах (1 Å=1·10-10 м), а энергию – в электронвольтах. В этих единицах радиальное уравнение Шредингера и эффективная потенциальная функция принимают вид:
 , ,
| (6.30) |
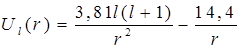 . .
| (6.31) |
Для решения дифференциального уравнения (6.30) используется алгоритм Эйлера – Кромера. Два краевых условия, необходимых для реализации алгоритма, в случае s-задачи задаются при r=0: значение волновой функции f(0)=0 и отличное от нуля значение ее первой производной f '(0)≠0. Поскольку в p- и d-состояниях в центре обращается в нуль не только волновая функция, но и ее первая производная, то их значения приходится задавать на некотором небольшом удалении от центра (порядка 0,01 Å).
Ход решения отображается на дисплее либо графиком волновой функции f ( r ), либо графиком радиальной плотности вероятности f 2(r). Эти графики для разных уровней энергии E располагаются каждый в своей системе координат. Их оси абсцисс, вдоль которых в относительных единицах откладываются f ( r ) или f 2(r) берут начало на соответствующих уровнях энергии.
Поиск физически приемлемых решений состоит в нахождении методом проб и ошибок таких значений энергии E, при которых график волновой функции не расходится в заданных пределах изменения радиальной координаты. Процесс поиска облегчает то обстоятельство, что при отклонении E от собственного значения в большую или меньшую сторону волновая функция расходится (т. е. неограниченно возрастает) в разных направлениях (вверх либо вниз).
Порядок выполнения работы
Проверочные вопросы
Чтобы перейти к выполнению лабораторной работы необходимо ответить на несколько проверочных вопросов. Кнопка «Основные вопросы теории и как управлять программой» открывает файл справки, который поможет в случае затруднений ответов на вопросы.
Каждый вопрос находится на отдельной закладке, имя которой соответствует номеру вопроса. Переключая закладки, можно получить доступ к любому вопросу. После того, как вы ответили на все вопросы, нужно нажать кнопку «Готово». Если вы ответили на все вопросы правильно, то откроется главное окно программы, и вы можете приступить к выполнению работы. Если вы ответили неправильно хотя бы на один вопрос, то вы не сможете выполнять работу до тех пор, пока не найдете и не исправите ошибку.
Ответ на вопрос отмечается значком возле правильных вариантов ответа (их может быть несколько).
Управление программой
При запуске программы появляется заглавное окно. После этого, нажав кнопку «Ok», следует ответить на проверочные вопросы. Затем открывается главное окно программы, в котором слева находится панель ввода данных, справа – окно вывода, сверху – меню и панель инструментов.
Программа может работать в двух режимах: ручном и автоматическом. В ручном режиме студент самостоятельно задает значение энергии E, а программа строит волновую функцию, соответствующую этому значению. В автоматическом режиме программа сама находит уровни энергии E и строит соответствующие им волновые функции. Значения этих уровней энергии выводятся в таблицу. Чтобы автоматический режим стал доступен, нужно найти несколько уровней энергии E в ручном режиме.
Процесс поиска уровня энергии E заключается в следующем: величину энергии E изменяют до тех пор, пока при значении E чуть меньше предыдущего волновая функция не будет расходиться (неограниченно расти при  ) в одном направлении, а при значении E чуть больше предыдущего – в противоположном. Ширину этой «вилки» сужают настолько, чтобы она сравнялась с требуемой точностью значения E (четыре знака после запятой).
) в одном направлении, а при значении E чуть больше предыдущего – в противоположном. Ширину этой «вилки» сужают настолько, чтобы она сравнялась с требуемой точностью значения E (четыре знака после запятой).
В компьютерной программе решение уравнения Шредингера предваряется построением графика зависимости эффективной потенциальной энергии Ul от r. На график наносится масштабная сетка вертикальных линий с шагом, равным значению первого боровского радиуса, с помощью которой можно выполнять количественную оценку размеров электронных «облаков».
Панель ввода данных состоит из поля ввода значений энергии E, переключателя задач и измерителя радиальной координаты. Для ввода значения энергии E следует набрать некоторое вещественное число и нажать клавишу «Enter», после чего программа построит соответствующую волновую функцию.
В группе «Задачи» переключение осуществляется с помощью мыши или управляющих клавиш: «Стрелка вверх» или «Стрелка вниз».
С помощью измерителя радиальной координаты можно определять размер атома водорода в различных стационарных состояниях.
Переключаться между группой «Задачи», полем ввода для энергии и измерителем радиальной координаты можно с помощью клавиши «Tab» или мыши.
Окно вывода предназначено для отображения одного или нескольких графиков волновой функции. По умолчанию окно размещается на экране, благодаря чему можно видеть всю картину. Используя команду «Размещать окно в экране» в меню «Настройки», можно увеличить размер окна, а, следовательно, и масштаб графиков. Тогда изображение можно прокручивать или «таскать» мышкой. Это удобно, если вы хотите рассмотреть мелкие детали. Если флажок с команды меню «Размещать окно в экране» снят, то размер окна можно изменять, используя команду «Размер окна».
В меню «Программа» «Справка» – открывает файл справки (теория, задание, управление программой), «Описание» – название лабораторной работы, «Выход» – выход из программы.
В меню “Настройки» «Квадрат волновой функции» – строит графики квадрата волновой функции, «Сравнить все три задачи» – отображает три ямы вместе с волновыми функциями для их сравнения, «Размещать окно в экране» – позволяет изменять размеры окна вывода командой «Размеры окна».
В Меню “Изображение” команда «Сохранить в файл» позволяет сохранять изображение в окне вывода на диск. Для этого необходимо ввести имя файла и сохранить его. Команда «Распечатать» позволяет распечатать на принтере изображение из окна вывода.
Задание
1. Провести численное решение радиального уравнения для s-, p-, и d- задач. Найти уровни энергии и радиальные функции для четырех s-состояний, трех p-состояний и двух d-состояний.
2. Зарисовать картину уровней энергии и графики радиальных функций f(r) и R(r), а также графики распределения радиальной электронной плотности. Установить, имеет ли место вырождение уровней по квантовому числу l.
3. Пользуясь масштабной сеткой, оценить (в боровских радиусах) размеры «электронных облаков» для различных состояний. Выявить основные закономерности, характеризующие зависимость вида распределения радиальной электронной плотности от квантовых чисел n и l.
4. Оценить энергию и размеры атома водорода для состояний 2p, 3d и 4f, используя лишь выражение (14) для эффективной потенциальной энергии .
5. Кнопкой «Электронные облака атома водорода» вызвать соответствующую программу, и с ее помощью рассмотреть радиально-угловые распределения электронной плотности для состояний 1s, 2s, 3s, 4s, 2p, 3p, 4p, 3d, 4d, 4f. Зарисовать двухмерные картинки для этих состояний, а также графики распределения радиальной электронной плотности (последние вызываются кнопкой 2D).
Установить, сколько различных распределений существует при заданных n и l и сколько, если задано только n. Сравнить эти результаты с кратностью вырождения уровня.
Контрольные вопросы
1. Какому дифференциальному уравнению и каким условиям удовлетворяют волновые функции, описывающие стационарные состояния электрона в атоме водорода?
2. Каким образом трехмерная задача о поведении электрона в атоме водорода сводится к набору одномерных квантовомеханических задач? Какие значения принимают квантовые числа l и ml?
3. Какой вид имеют волновые функции в состояниях с определенными значениями E , L 2 , Lz?
4. С помощью какого уравнения можно найти радиальные функции и уровни энергии?
5. Как вводится главное квантовое число n? Какие значения может принимать число n при заданном l? Число l при заданном n?
6. Что такое кратность вырождения уровня? Чему равны кратности вырождения уровней энергии атома водорода?
7. Какие квантовые числа определяют зависимость электронной плотности от углов? От радиальной координаты?
8. Как изменяется распределение радиальной электронной плотности с изменением n и l ? Чему равно число максимумов этого распределения при заданных n и l?
9. Чему равен первый боровский радиус?
10. Как изменяется угловое распределение электронной плотности с увеличением модуля m при заданном l?
11. Почему все рассмотренные распределения не зависят от угла φ и от знака m?
Дата добавления: 2021-04-05; просмотров: 104; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
