ИССЛЕДОВАНИЕ ТЕРМОДИНАМИЧЕСКИХ ЦИКЛОВ
Федеральное государственное автономное образовательное учреждение высшего образования «Санкт-Петербургский государственный электротехнический университет «ЛЭТИ»
им. В.И. Ульянова (Ленина)»
кафедра физики
ОТЧЕТ
По лабораторной работе №9
«ИССЛЕДОВАНИЕ ТЕРМОДИНАМИЧЕСКИХ ЦИКЛОВ»
Выполнил: Хамитов Камиль Азатович
Группа №: 9205
Преподаватель: Черемухина Ирина Анатольевна
Санкт-Петербург, 2019
ЛАБОРАТОРНАЯ РАБОТА №9
ИССЛЕДОВАНИЕ ТЕРМОДИНАМИЧЕСКИХ ЦИКЛОВ
 Цель работы: исследование политропно-изохорно-изотермического (nVT) и адиабатно-изохорно-изотермического (SVT) циклов.
Цель работы: исследование политропно-изохорно-изотермического (nVT) и адиабатно-изохорно-изотермического (SVT) циклов.
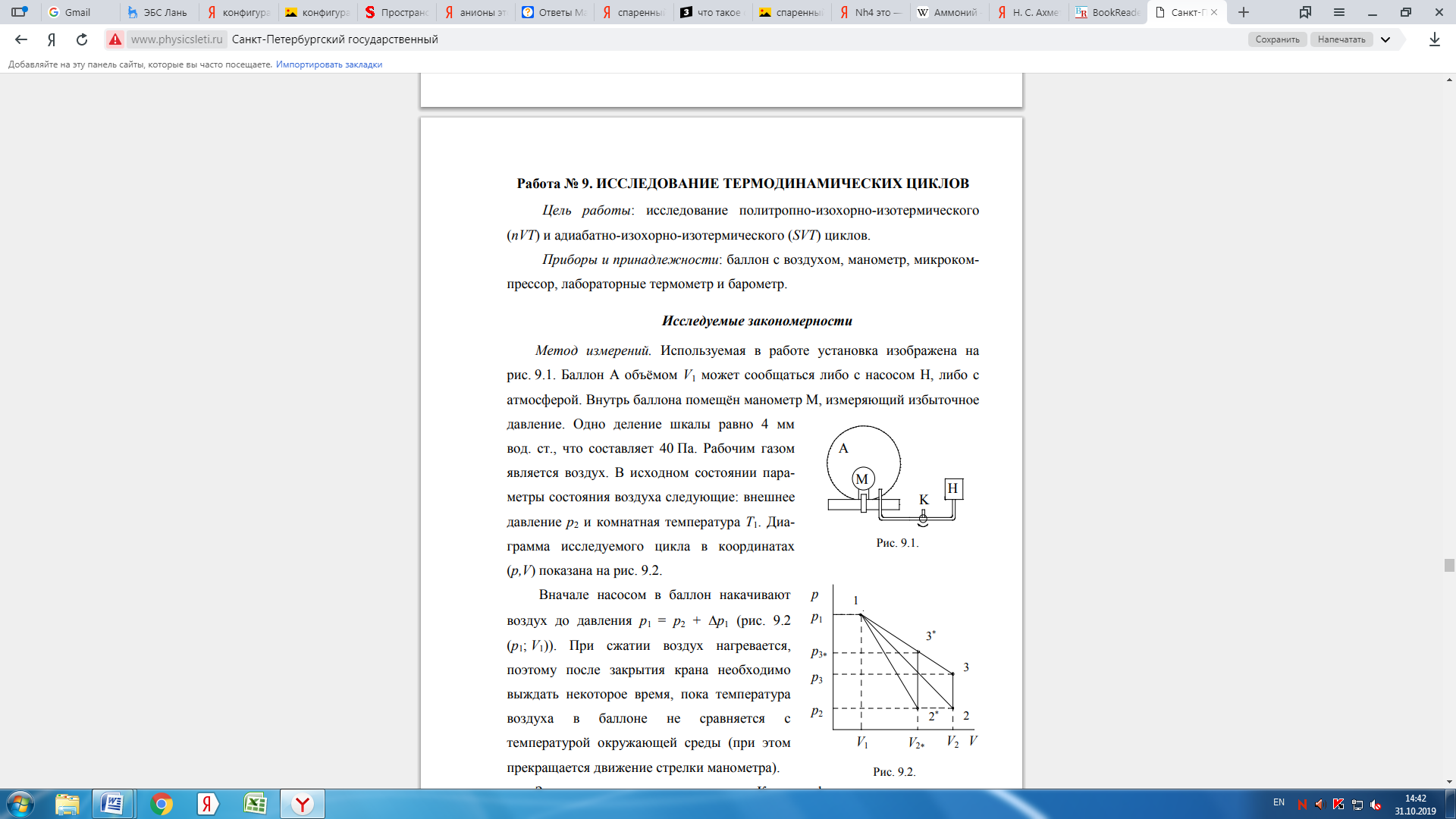
Приборы и принадлежности: баллон с воздухом(на рис.-А), манометр(на рис.-М), микрокомпрессор(на рис.-Н), лабораторные термометр и барометр.
Исследуемые закономерности:
Метод измерений. Используемая в работе установка изображена на рисунке справа. Баллон А объёмом  может сообщаться либо с насосом H, либо с атмосферой. Внутрь баллона помещён манометр М, измеряющий избыточное давление. Одно деление шкалы равно 4 мм вод. ст., что составляет 40 Па. Рабочим газом является воздух. В исходном состоянии параметры состояния воздуха следующие: внешнее давление
может сообщаться либо с насосом H, либо с атмосферой. Внутрь баллона помещён манометр М, измеряющий избыточное давление. Одно деление шкалы равно 4 мм вод. ст., что составляет 40 Па. Рабочим газом является воздух. В исходном состоянии параметры состояния воздуха следующие: внешнее давление 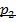 и комнатная температура
и комнатная температура 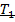 .
.
· Диаграмма исследуемого цикла в координатах (p,V) показана на рисунке ниже 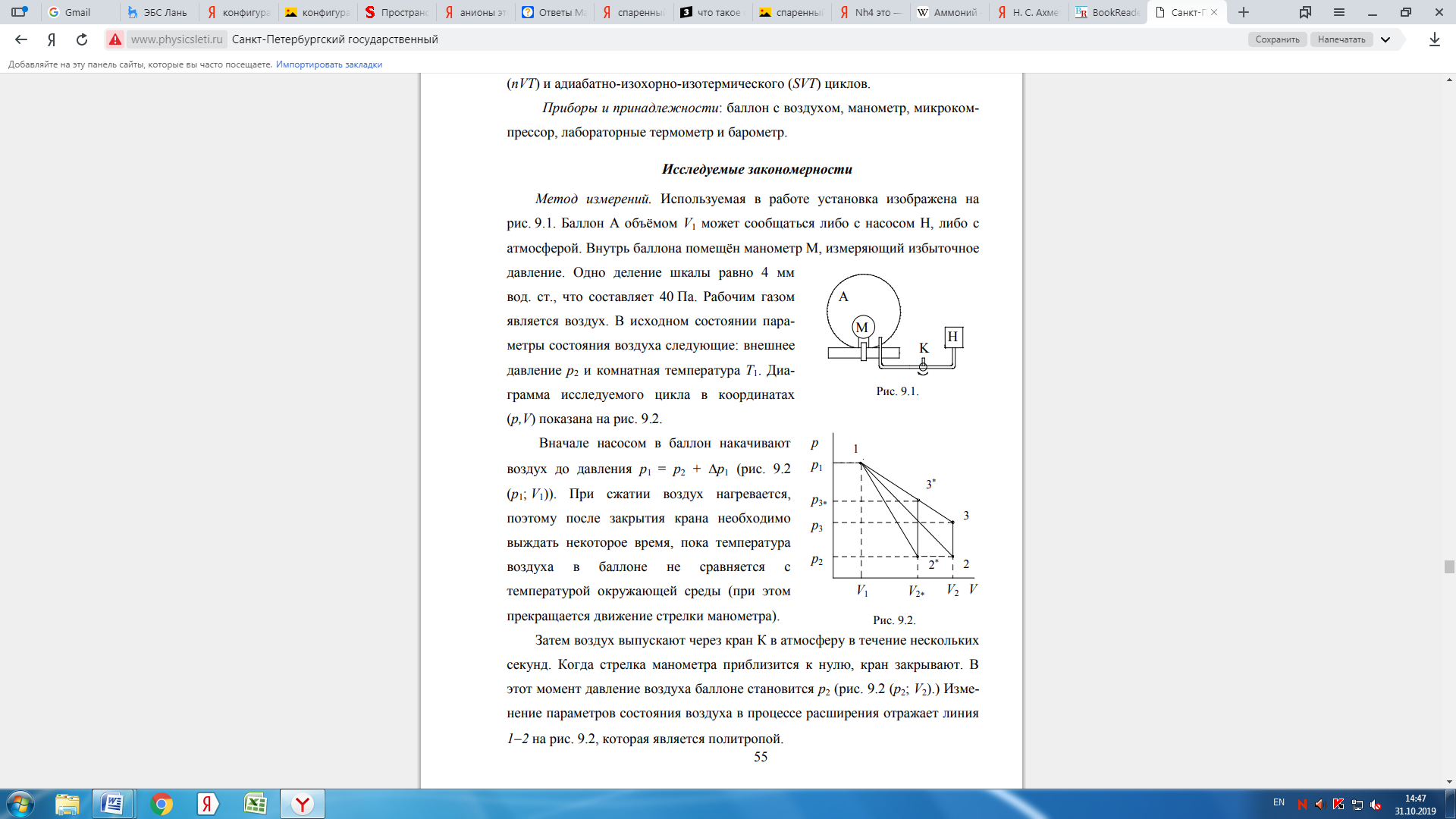 первого.
первого.
|
|
|
1. Вначале насосом в баллон накачивают воздух до давления 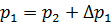 (координаты в осях на графике (
(координаты в осях на графике ( 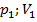 )). ! При сжатии воздух нагревается, поэтому после закрытия крана необходимо выждать некоторое время, пока температура воздуха в баллоне не сравняется с температурой окружающей среды (при этом прекращается движение стрелки манометра)!
)). ! При сжатии воздух нагревается, поэтому после закрытия крана необходимо выждать некоторое время, пока температура воздуха в баллоне не сравняется с температурой окружающей среды (при этом прекращается движение стрелки манометра)!
2. Затем воздух выпускают через кран К в атмосферу в течение нескольких секунд. Когда стрелка манометра приблизится к нулю, кран закрывают. В этот момент давление воздуха баллоне становится 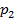 (координаты в осях на графике (
(координаты в осях на графике ( 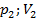 ))Изменение параметров состояния воздуха в процессе расширения отражает линия 1 - 2 на графике, которая является политропой.
))Изменение параметров состояния воздуха в процессе расширения отражает линия 1 - 2 на графике, которая является политропой.
3. После закрытия крана охлаждённый при расширении воздух изохорически нагревается до температуры окружающей среды в результате теплообмена с ней. Изменение параметров состояния воздуха отражает линия 2-3 на графике, которая является изохорой. Температура воздуха в баллоне становится равной температуре в точке 1 ( 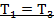 ), следовательно, точки 1 и 3 лежат на одной изотерме!
), следовательно, точки 1 и 3 лежат на одной изотерме!
4. После выравнивания температур давление в баллоне изменится на 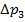 и станет
и станет 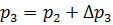 (на графике
(на графике 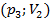 ). Таким образом,
). Таким образом, 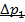 и
и 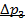 - это изменения давления на участках 1 - 2 и 2 - 3. Участки 1 - 2 и 1 - 3 на диаграмме можно аппроксимировать прямыми, так как изменения параметров p, V, T в данной работе малы и много меньше абсолютных значений соответствующих величин.
- это изменения давления на участках 1 - 2 и 2 - 3. Участки 1 - 2 и 1 - 3 на диаграмме можно аппроксимировать прямыми, так как изменения параметров p, V, T в данной работе малы и много меньше абсолютных значений соответствующих величин.
|
|
|
В работе изучается политропно-изохорно-изотермический (nVT) цикл. Для сравнения с nVT циклом используется адиабатно-изохорно-изотермический (SVT) цикл, отличающийся тем, что процесс расширения газа на участке 1 - 2* рассматривается как адиабатический. Изучение циклов осуществляется путем их моделирования при значениях показателя адиабаты γ=1,4 и показателя политропы n, определенным опытным путем.
Определение показателя политропы: Первое начало термодинамики формулируется следующим образом: сообщённое системе количество теплоты d Q расходуется на увеличение внутренней энергии dU системы и совершение системой работы d А:
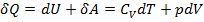
Где 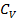 – теплоемкость газа в изохорном процессе.
– теплоемкость газа в изохорном процессе.
v nVT-цикл .
Процесс расширения воздуха на участке 1-2 (на графике) является политропным, в котором теплоёмкость газа С =const. Первое начало термодинамики для политропного процесса имеет вид:

где C – теплоемкость воздуха в политропном процессе,  .
.
|
|
|
ü Из этого соотношения с помощью уравнения состояния идеального газа можно получить уравнение Пуассона для политропного процесса:
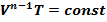 или
или  , где n – показатель политропы,
, где n – показатель политропы,
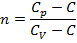
где 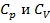 - теплоемкости газа в изобарном и изохорном процессах.
- теплоемкости газа в изобарном и изохорном процессах.
v SVT-цикл.
Предположим, что процесс расширения воздуха на участке 1-2 * (на графике)
является адиабатным. Адиабатный процесс является одним из видов политропных процессов, он происходит без теплообмена с окружающей средой: d Q = 0 и теплоемкость газа в этом процессе С = 0. Поэтому показатель политропы в этом процессе равен  и называется показателем адиабаты. Взаимосвязь между параметрами состояния в адиабатном процессе также описывается уравнениями Пуассона либо объединенным газовым законом.
и называется показателем адиабаты. Взаимосвязь между параметрами состояния в адиабатном процессе также описывается уравнениями Пуассона либо объединенным газовым законом.
Показатель политропы n может быть определён экспериментально. Выразим n через экспериментально измеряемые величины, для чего продифференцируем уравнения политропы (  ) и изотермы (рV = const):
) и изотермы (рV = const): 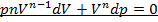 - для политропы и р dV + V dр = 0 - для изотермы. Откуда:
- для политропы и р dV + V dр = 0 - для изотермы. Откуда:
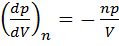
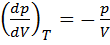
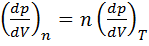
При относительно малых изменениях D p и D V угловые коэффициенты политропы 1-2 и изотермы 1-3 (на графике) рассчитывается по формулам
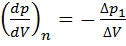
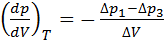
|
|
|
где DV = 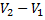 . Из этих и приведенных выше соотношений получаем формулу
. Из этих и приведенных выше соотношений получаем формулу
 .
.
Зная n, можно определить мольную теплоемкость газа в политропном процессе (мольные величины обозначаем соответствующими строчными буквами)
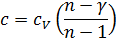
Где  – показатель адиабаты, равный отношнию теплоемкостей газов в изобарном и изохорном процессах,
– показатель адиабаты, равный отношнию теплоемкостей газов в изобарном и изохорном процессах, 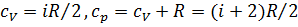 , где i – число степеней свободы молекул газа, R – универсальная газовая постоянная. Воздух можно считать двухатомным газом. Для которого при небольших температурах i = 5,
, где i – число степеней свободы молекул газа, R – универсальная газовая постоянная. Воздух можно считать двухатомным газом. Для которого при небольших температурах i = 5, 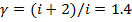
· На участке 1-2 воздух охлаждается, а тепло через стеклянную колбу поступает в систему ( dQ > 0 , dT < 0 ) поэтому теплопоемкость газа в политропном процессе 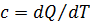 – отрицательна. Это означает согласно формуле (2), что на участке 1–2 показатель политропы
– отрицательна. Это означает согласно формуле (2), что на участке 1–2 показатель политропы 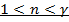 .
.
v Расчет изменения внутренней энергии и работы газа на участках цикла.
Так как в цикле и в изотермическом процессе 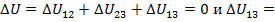 0 , то изменение внутренней энергии газа в политропном процессе
0 , то изменение внутренней энергии газа в политропном процессе 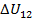 и в изохорном процессе
и в изохорном процессе 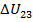 одинаковы по величине и противоположны по знаку. Тогда
одинаковы по величине и противоположны по знаку. Тогда 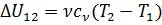 где ν – число молей воздуха в баллоне, определяемое по уравнению состояния (уравнение Менделеева-Клапейрона).
где ν – число молей воздуха в баллоне, определяемое по уравнению состояния (уравнение Менделеева-Клапейрона).
Работа расширения (сжатия) газа в политропическом 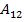 и изотермическом
и изотермическом  процессах может быть рассчитана по формулам:
процессах может быть рассчитана по формулам:
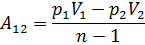
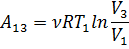
v Расчёт холодильного коэфициента.
Цикл, изучаемый в данной работе, является холодильным (ориентирован против часовой стрелки). Его эффективность принято характеризовать холодильным коэффициеном e, который определяется как отношение теплоты, отнятой от охлаждаемого газа, к затраченной в цикле работе. Для SVT-цикла с учетом 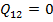 и
и  холодильный коэффициент e равен (обозначения цифровых индексов согласованы с графиком).
холодильный коэффициент e равен (обозначения цифровых индексов согласованы с графиком).

Для nVT-цикла в предположении 
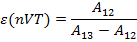
Перепишем выражения для e, используя экспериментально измеряемые величины давлений, для чего значения работы 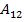 и
и 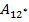 определим графическим способом. В рV-координатах (на графике) они равны площадям трапеций, основания которых
определим графическим способом. В рV-координатах (на графике) они равны площадям трапеций, основания которых 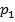 и
и  (либо
(либо 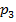 или
или 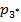 ), а высоты - (
), а высоты - ( 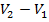 ) и (
) и ( 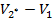 ) соответственно. Учитывая, что
) соответственно. Учитывая, что 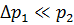 и
и  , получим
, получим
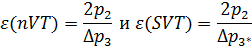
ü В проводимом опыте 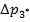 >
> 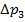 , поэтому отношение холодильных коэффициентов
, поэтому отношение холодильных коэффициентов  .
.
v Расчет изменения энтропии .
Функция состояния, дифференциалом которой является отношение dQ / T, называется энтропией:
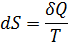
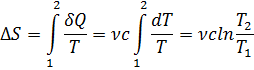
где c - мольная теплоемкость газа, зависящая от типа политропного процесса (адиабатный, изохорный, изобарный и т.п.). Отметим, что данное выражение справедливо лишь для обратимых процессов, то есть процессов, которые могут быть проведены в обратном направлении через те же промежуточные состояния, что и при прямом процессе; при этом тепловое состояние окружающей среды не изменяется (процесс без теплопотерь)
ü Выразим изменение энтропии D S через экспериментально определяемые в опыте величины давлений сначала для nVT-цикла.
Ø В политропном процессе (на участке 1-2) с учетом уравнения Пуассона 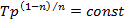
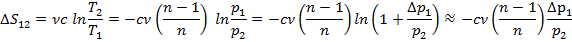
Ø В изохорном процессе (на участке 2-3) изменение энтропии с учетом 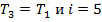 , а также уравнения Пуассона равно:
, а также уравнения Пуассона равно:
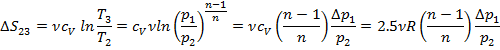
Ø В изотермическом процессе (на участке 3-1)
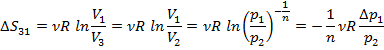
Для SVT-цикла изменение энтропии в адиабатном процессе (на участке 1- 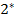 ) равно нулю. С учетом, что изменение энтропии в цикле также равно нулю, заключаем, что изменения энтропии в изохорном и изотермическом процессах равны по величине, но различаются знаком:
) равно нулю. С учетом, что изменение энтропии в цикле также равно нулю, заключаем, что изменения энтропии в изохорном и изотермическом процессах равны по величине, но различаются знаком:
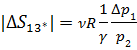
ПРОТОКОЛ НАБЛЮДЕНИЙ
ЛАБОРАТОРНАЯ РАБОТА №9
ИССЛЕДОВАНИЕ ТЕРМОДИНАМИЧЕСКИХ ЦИКЛОВ

| 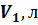
| 
| 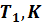
|
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | |
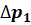
| ||||||||||
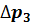
|
Выполнил: Хамитов Камиль Азатович
Факультет Электроники
Группа № 9205
Преподаватель: Черемухина Ирина Анатольевна
Дата добавления: 2021-06-02; просмотров: 268; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
