В конце курсовой работы студент помещает выводы, где подводит итог выполненной работы, анализирует входящие в цикл процессы, оценивает к.п.д. рассматриваемого цикла.
Методические указания к курсовой работе
на тему
«Анализ и расчет термодинамических циклов тепловых машин»
ОГЛАВЛЕНИЕ
1. Цель работы…………………………………………………………1
2. Содержание задания и исходные данные…………………………1
3. Подготовка к выполнению курсовой работы……………………..4
4. Порядок выполнения работы………………………………………8
5. Пример выполнения курсовой работы…………………………...12
6. Отчетность по работе……………………………………………...13
7. Контрольные вопросы…………………………………………….15
Литература..………………………………………………………..16
1. ЦЕЛЬ РАБОТЫ
Курсовая работа направлена на усвоение основных положений термодинамики и позволяет студентам не только глубже понять основные закономерности процессов преобразования теплоты в механическую работу, а, следовательно, и принцип действия тепловых машин, но и получить необходимые практические навыки выполнения расчетов и анализа термодинамических циклов тепловых машин.
2. СОДЕРЖАНИЕ ЗАДАНИЯ И ИСХОДНЫЕ ДАННЫЕ
При выполнении курсовой работы по термодинамике студенты рассчитывают замкнутый термодинамический процесс (цикл) по четырём составляющим его политропным участкам. По результатам расчета строятся графики цикла в р-v и Т-s координатах.
Задание на курсовую работу выдается каждому студенту индивидуально на специальном бланке (таблица 2.1), в котором приводятся необходимые для расчета исходные данные и общий вид рассчитываемого цикла в р-v координатах.
|
|
|
В процессе выполнения курсовой работы по исходным данным требуется определить:
1) параметры состояния рабочего тела (воздуха): давление р, удельный объём v, температуру Т и энтропию s во всех четырех узловых точках 1, 2, 3 и 4 данного цикла;
2) параметры состояния воздуха (p, v, T и s) в 2-3-х промежуточных точках для каждого из 4-х процессов цикла;
3) показатель политропы n для каждого процесса цикла, теплоёмкость cn и работу расширения (сжатия) l воздуха в рассчитываемом процессе, количество подведенной (отведенной) в нём теплоты q, а также изменение внутренней энергии Δu, изменение энтальпии Δi воздуха, коэффициент ψ распределения тепла между внутренней энергией и совершаемой воздухом работой в рассматриваемом процессе данного цикла;
4) работу lц воздуха за цикл, количество теплоты qподв, подведенной к воздуху извне за цикл, и теплоты qотв, отведенной от воздуха в охладитель в ходе совершения цикла, а также количество теплоты qц, превращенной в работу, изменения внутренней энергии Δuц, энтальпии Δiц и энтропии Δsц воздуха за цикл, термический к.п.д. ηt рассчитываемого цикла и термический к.п.д. ηtк, соответствующего ему цикла Карно.
|
|
|
Результаты расчетов вносятся в бланк задания и по ним строятся в соответствующем масштабе рабочая р-v (рис.2.1) и тепловая Т-s (рис.2.2) диаграммы рассчитанного термодинамического цикла.
Министерство науки и высшего образования РФ
Московский авиационный институт (Национальный исследовательский университет) МАИ
Кафедра «Технология производства и эксплуатации двигателей летательных аппаратов» Таблица 2.1
Студенту__________________________________институт________________группа___________________________
(фамилия, и., о.)
|
| Характерные точки | Промежуточные точки | Диа-грамма | ||||||||||
| 1 | 2 | 3 | 4 | 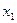 ; ; 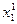
| x2 ; 
| x3 ; 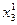
| x4 ; 
| x5 ; 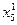
| x6 ; 
| ||||
| р, МПа | 0,08 | 3,92 | p – v | ||||||||||
| v, м3/кг | |||||||||||||
| T, К | 280 | T – s
| |||||||||||
| s, кДж/(кг·К) | |||||||||||||
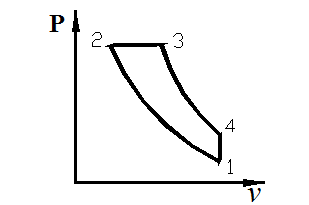
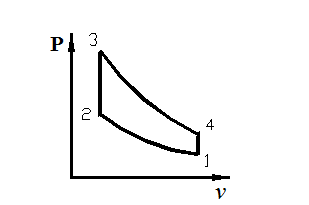 Произвести расчёт и анализ
Произвести расчёт и анализ
термодинамического цикла
| Для процесса | n | с кДж/(кг·К) | l кДж/кг | q кДж/кг | Du кДж/кг | Di кДж/кг | Ds кДж/(кг·К) | y = 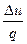
|
| 1-2 | к | |||||||
| 2-3 | 0 | 1465 | ||||||
| 3-4 | ||||||||
| 4-1 | +∞ |
Рабочее тело – воздух, в количестве 1 кг.
Для воздуха:
R = 0,287 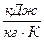
сv = 0,712 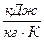 .
.
Определить величины:
а) p ; v ; T и s , для характерных точек цикла;
| Для цикла | qподв кДж/кг | qотв кДж/кг | lц кДж/кг | qц кДж/кг | Δuц кДж/кг | Δiц кДж/кг | Δsц кДж/(кг·К) | h t |
б) n ; c ; l ; q ; D u ; D i ; D s и y для процессов
цикла;
в) q подв; q отв; l ц; q ц; Du ц; Di ц; Ds ц и h t для цикла целом.
Дополнительные данные: v1 = 12v 2
Выдано « » ___________ 20 г. Принято «_____» __________________20 г. Преподаватель ________________________
3. ПОДГОТОВКА К ВЫПОЛНЕНИЮ КУРСОВОЙ РАБОТЫ
|
|
|
Приступая к выполнению курсовой работы, студенты должны проработать разделы, посвященные первому и второму законам термодинамики, а также исследованию политропных процессов и циклов, т.е. должны знать следующие основные соотношения термодинамики, справедливые для идеальных газов [1]:
1. Уравнение состояния идеального газа
р v = RT, (1)
где R – удельная газовая постоянная.
2. Уравнение политропного термодинамического процесса
р v n = const, (2)
где n – показатель политропы, равный
n =  . (3)
. (3)
Здесь и далее индексами «1» и «2» обозначены параметры состояния газа соответственно в начале и в конце рассматриваемого процесса.
3. Уравнение первого закона термодинамики
q = Δu + l. (4)
Здесь Δu – изменение внутренней энергии, которое для всех процессов идеального газа равно
Δu = u2 – u1 = cv (T2 – T1), (5)
где cv – теплоемкость газа в процессе при постоянном объёме, а
l – работа расширения (сжатия) газа, которая во всех процессах, кроме изотермического, может быть определена из выражения
l =  (Т2 – Т1). (6)
(Т2 – Т1). (6)
Работа газа в изотермическом процессе равна
l = RT·ln 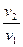 = RT·ln
= RT·ln  . (7)
. (7)
Для определения работы газа в адиабатном процессе (q=0 кДж/(кг К)) можно воспользоваться выражением 1 закона термодинамики, тогда
l = -Δu = cv (T1 – T2). (8)
Изменение энтальпии для всех процессов идеального газа равно
Δi = i2 – i1 =cp (T2 – T1), (9)
где в соответствии с формулой Майера теплоёмкость газа в процессе при постоянном давлении равна
cp = cv + R. (10)
4. Уравнение для определения количества теплоты
q = cn (T2 – T1), (11)
где cn – теплоемкость газа в политропном процессе, равная
cn = cv +  , (12)
, (12)
или
cn = cv  . (13)
. (13)
Здесь k – показатель адиабаты, равный k =  , для воздуха k=1,4.
, для воздуха k=1,4.
5. Аналитическое выражение второго закона термодинамики:
ds = 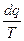 , (14)
, (14)
или Δs = s2 – s1 = cn·ln  , (15)
, (15)
и Δs = s2 – s1 = cp·ln  R·ln
R·ln 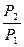 . (16)
. (16)
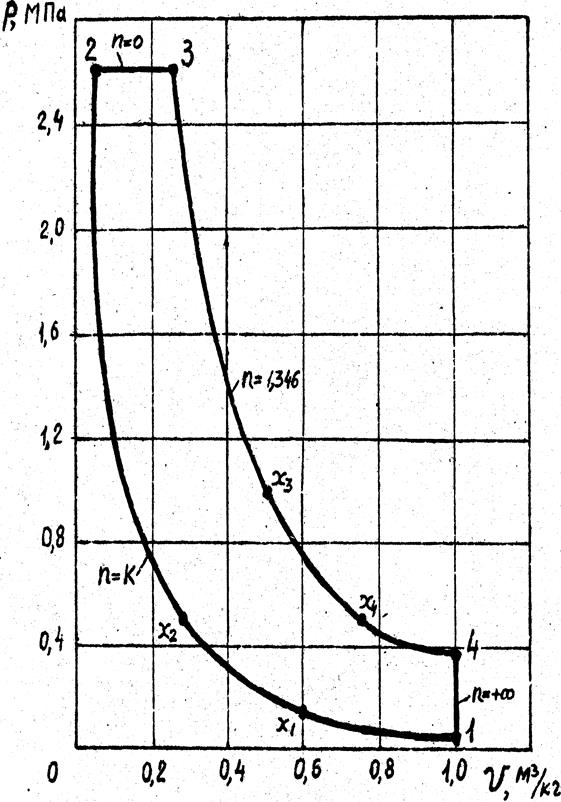
Рис.2.1. Рабочая диаграмма цикла.

Рис. 2.2. Тепловая диаграмма цикла
4. ПОРЯДОК ВЫПОЛНЕНИЯ РАБОТЫ
Расчет термодинамического цикла по четырем составляющим его политропным процессам для идеальных газов (воздуха) состоит в применении к ним рассмотренных выше основных соотношений термодинамики.
Выполнение курсовой работы следует начинать с составления плана проведения расчетов. В зависимости от исходных данных производят либо последовательный расчет параметров воздуха от точки 1 до точки 4 цикла, либо сначала определяют параметры воздуха в точках 1, 2, и 4, и лишь затем в точке 3 цикла. В остальном порядок проведения расчетов для различных вариантов задания не имеет существенных различий. Он включает в себя пять основных этапов.
1. Расчет параметров воздуха (p, v, T, s) в узловых точках цикла.
Порядок расчета следующий:
а) определяют начальное состояние воздуха в точке 1, при этом давление, удельный объём или температура вычисляются по формуле (1), а энтропия воздуха – по формуле (16). При этом считают, что для физических условий (Т0=273 К, p0=105 Н/м2), энтропия s0 = 0 кДж/(кг К). Тогда формула (16) имеет вид:
s1 – s0 = s1 = cP·ln  - R·ln
- R·ln  ; (17)
; (17)
б) определяют состояние воздуха в точке 2, при этом давление, удельный объём или температура воздуха находятся из уравнений (1) и (2).
Расчетные зависимости имеют следующий вид:
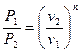 ; (18)
; (18)
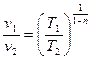 ; (19)
; (19)
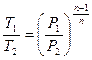 . (20)
. (20)
Энтропия воздуха в точке 2 определяется из уравнения (15) или (16):
s2 = s1 + cn·ln  ,
,
или
s2 = s1 + cР·ln  - R·ln
- R·ln 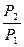 .
.
Аналогично рассчитывают параметры состояния воздуха и в других узловых точках цикла. При этом, если заданными являются величины Δu2-3, Δi2-3 или q2-3, то сначала из уравнений (5), (9) или (11) определяют температуру воздуха в точке 3, а затем по заданным величинам давления или удельного объёма, используя уравнения (1), (15) или (16), вычисляют остальные параметры в точке 3 цикла.
Основные параметры в точке 4 определяют или из уравнений (18-20), описывающих связи между параметрами газа в точках 3 и 4 (когда в точке 4 задан лишь один параметр из трёх и задан показатель политропы n3-4), или непосредственно из уравнения состояния (когда в точке 4 заданы два параметра из трёх). При этом, если в последнем случае задаются также показатель политропы n3-4 и лишь один параметр воздуха в точке 3, то состояние воздуха в этой точке цикла определяют после точки 4, используя уравнения (18-20).
2. Расчет параметров воздуха (p, v , Т, s) в промежуточных точках процессов цикла.
Промежуточные точки назначаются студентами самостоятельно и раздельно для рабочей р-v и тепловой Т-s диаграмм цикла таким образом, чтобы на каждом криволинейном участке диаграммы было не менее 2-х точек.
Принятые промежуточные точки обозначаются через 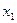 ,
,  и т.д. для рабочей р-v и
и т.д. для рабочей р-v и  ,
, 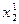 и т.д. для тепловой Т-s диаграмм цикла. Параметры состояния воздуха в промежуточных точках цикла вычисляются по формулам (18) и (15), которые при принятых обозначениях принимают следующий вид:
и т.д. для тепловой Т-s диаграмм цикла. Параметры состояния воздуха в промежуточных точках цикла вычисляются по формулам (18) и (15), которые при принятых обозначениях принимают следующий вид:
 = р1
= р1 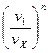 , (21)
, (21)
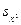 = s1 + cnln
= s1 + cnln 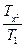 , (22)
, (22)
где значениями удельного объёма vx в точке x и температуры  в точке х1 цикла следует задаваться при расчете таким образом, чтобы промежуточные точки равномерно располагались на исследуемом участке диаграммы.
в точке х1 цикла следует задаваться при расчете таким образом, чтобы промежуточные точки равномерно располагались на исследуемом участке диаграммы.
3. Построение рабочей (р-v ) и тепловой (T-s) диаграмм цикла. Графики строят по узловым и промежуточным точкам, имея при этом в виду, что:
- цикл как в рабочей р-v, так и в тепловой Т-s диаграммах, изображается замкнутой кривой, причем направление процессов цикла в этих диаграммах одинаково – по ходу движения часовой стрелки;
- все политропные процессы в тепловой диаграмме представляются логарифмическими кривыми, направленными выпуклостью вниз;
- расположение политропных процессов в рабочей диаграмме зависит от величины показателя политропы: при ∞>n>0, как это следует из уравнения (18), политропа имеет гиперболический характер; при 0>n>- ∞ политропы представляют собой кривые, проходящие через начало координат, причем при n > -1 кривая процесса направлена выпуклостью вверх, а при n < -1 направлена выпуклостью вниз, в частности при n = -1 политропа является прямой линией.
4. Определение величин, характеризующих процессы цикла:
а) показатель политропы вычисляется по формуле (3);
б) теплоёмкость воздуха в рассматриваемом процессе определяется по формуле (12) или (13), причем теплоёмкость отрицательна, если 1<n<k;
в) работа, производимая воздухом в политропном процессе, определяется по одному из выражений (6), (7) или (8); полученная величина должна быть численно равна площади под кривой этого процесса в (р-v) диаграмме. Работа считается положительной при расширении газа и отрицательной при сжатии газа;
г) количество подводимой (или отводимой) теплоты в политропном процессе вычисляется по формуле (4) или (11);
Найденная величина должна быть численно равна площади под кривой процесса в (T-s) диаграмме. Согласно уравнению (14), теплота подводится к газу извне (т.е. она положительная), если энтропия увеличивается (ds>0) и, наоборот, теплота отводится от газа в окружающую среду (т.е. она отрицательная), если энтропия уменьшается (ds<0).
д) изменение внутренней энергии воздуха для процесса определяется по формуле (5);
е) изменение энтальпии воздуха определяется по формуле (9);
ж) изменение энтропии определяется по формулам (15) или (16);
з) коэффициент распределения тепла между внутренней энергией и совершаемой работой воздуха за процесс находится по формуле:
ψ = 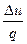 . (23)
. (23)
5. Определение величин, характеризующих цикл в целом:
а) работа воздуха за цикл определяется алгебраической суммой работ, совершенных газом в отдельных процессах цикла:
lц = l1-2 + l2-3 + l3-4 + l4-1 = ∑ li ; (24)
в соответствии с этим выражением за один цикл воздух совершает полезную работу, равную площади цикла, представленного в рабочей (р-v)диаграмме;
б) количество теплоты, превращенной в работу цикла, равно:
qц = qподв – qотв, (25)
где qподв – теплота, подведенная к газу извне за цикл, а qотв – теплота, отведенная от газа в охладитель в ходе совершения цикла.
Из уравнения (25) видно, что теплота цикла qц, превращенная в работу цикла lц, определяется площадью цикла в (T-s) диаграмме. Следовательно, площади цикла в (р-v) и (T-s) диаграммах имеют одинаковые значения;
в) изменение внутренней энергии, энтальпии и энтропии воздуха за цикл равно нулю, так как конечное состояние газа в результате совершения цикла совпадает с начальным состоянием, поэтому:
Δuц = Δu1-2 + Δu2-3 + Δu3-4 + Δu4-1 = 0 кДж/кг, (26)
Δiц = Δi1-2 + Δi2-3 + Δi3-4 + Δi4-1 = 0 кДж/кг, (27)
Δsц = Δs1-2 + Δs2-3 + Δs3-4 + Δs4-1 = 0 кДж/(кг К) (28)
г) термический к.п.д. цикла, который характеризует степень совершенства преобразования теплоты в работу, равен отношению полезной работы lц к подведенной теплоте qподв:
ηt = 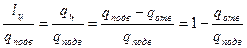 . (29)
. (29)
Из этого выражения следует, что термический к.п.д. цикла, представленного в (T-s) диаграмме, определяется отношением площади цикла к площади, соответствующей количеству подводимой теплоты.
Совершенство произвольного обратимого цикла оценивается сравнением его термического к.п.д. с термическим к.п.д. обратимого цикла Карно, осуществляемого между крайними (Tmax и Tmin) температурами рассматриваемого цикла.
Цикл Карно имеет максимальный термический к.п.д. для заданного интервала температур, равный:
ηtk = 1 -  . (30)
. (30)
Если сравнить рассчитываемый цикл с описанным вокруг него циклом Карно в (Т-s) диаграмме, то площадь рассматриваемого цикла получается меньше площади цикла Карно. Отношение этих площадей показывает насколько близко приближается рассматриваемый цикл к циклу Карно, т.е. определяют насколько термический к.п.д. рассматриваемого цикла меньше термического к.п.д. цикла Карно:
 .
.
5. ПРИМЕР ВЫПОЛНЕНИЯ КУРСОВОЙ РАБОТЫ
Ниже приводится порядок выполнения курсовой работы на примере варианта задания, исходные данные которого представлены в таблице 2.1. План проведения расчетов следующий.
1. Расчет параметров p,v,T,s в узловых точках цикла:
а) начальное состояние воздуха в точке 1 согласно исходным данным и формулам (1) и (17) составляет:
Р1 = 0,08 МПа = 0,8·105 Н/м2; Т1 = 280 К;
v 1 = 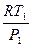 =
=  = 1,0045 м3/кг;
= 1,0045 м3/кг;
s1 = cp·ln 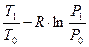 = 0,999∙ln
= 0,999∙ln 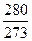 - 0,287∙ln
- 0,287∙ln 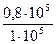 = 0,092 кДж/(кг∙К),
= 0,092 кДж/(кг∙К),
где согласно формуле (10)
сp = сv + R = 0,712 + 0,287 ≈ 0,999 кДж/(кг∙К);
б) состояние воздуха в точке 2 можно определить, используя соотношение  , когда сначала по вычисленному значению v1 находится удельный объём v 2, а затем по формуле (18) - давление Р2; температура Т2 находится из уравнения состояния (1);
, когда сначала по вычисленному значению v1 находится удельный объём v 2, а затем по формуле (18) - давление Р2; температура Т2 находится из уравнения состояния (1);
так как процесс 1-2 адиабатный (n = k), то изменение энтропии в этом процессе Δs1-2 = 0 (теплоемкость для адиабатного процесса сn= 0) и энтропия постоянна s2 = s1;
в) учитывая далее, что процесс 2-3 является изобарным (n = 0), находим давление Р3 = Р2, а так как при этом теплоёмкость cn = cp, то по
формуле (11) по заданному значению q2-3 и известной температуре Т2
вычисляем температуру воздуха Т3 в точке 3 цикла; энтропию s3 находим по формуле (15) или (17);
г) учитывая, что процесс 4-1 изохорный (n = + ∞), находим удельный объём воздуха v 4 = v 1, а далее по заданному значению Р4 и вычисленному значению v 4 определяем температуру Т4 в точке 4 цикла, энтропию воздуха s4 вычисляем по формуле (15) или (17), учитывая при этом, что теплоёмкость газа в процессе 4-1 cn = cv.
2. Расчет параметров p, v,T,s в промежуточных точках процессов цикла (см. п.2, раздел 4).
3. Построение рабочей (p- v) и тепловой (T-s) диаграмм цикла. По вычисленным значениям параметров состояния воздуха в узловых и промежуточных точках цикла в масштабе строятся рабочая (рис.2.1.) и тепловая (рис.2.2.)диаграммы цикла.
4. Определение величин, характеризующих процессы цикла (см. п.4, раздел 4).
5. Определение величин, характеризующих цикл в целом (см. п.5, раздел 4).
Результаты расчетов сводятся в общую таблицу 5.1.
6. ОТЧЕТНОСТЬ ПО РАБОТЕ
При защите курсовой работы студент должен представить пояснительную записку, оформленную соответствующим образом, и уметь ответить на вопросы, касающиеся содержания выполненной работы, обоснования используемых уравнений, а также на вопросы, связанные с термодинамическими особенностями процессов цикла (см. раздел 7).
Пояснительная записка должна содержать:
- оформленный и заполненный результатами расчетов бланк задания на курсовую работу (см. таблицу 5.1.);
- расчеты величин параметров состояния рабочего тела (воздуха) во всех узловых и промежуточных точках цикла, а также величин, характеризующих каждый из процессов цикла и цикл в целом. Все вычисления должны сопровождаться краткими пояснениями выбора расчетных формул и определения вспомогательных величин;
- рабочую и тепловую диаграммы цикла (см. рис.2.1 и рис.2.2).
Все расчеты выполняются в системе СИ: давление измеряется в н/м2 или в Па; температура Т - в К; удельный объём v - в м3/кг; теплота q, внутренняя энергия u и энтальпия i - в кДж/кг; теплоёмкость cn, энтропия и газовая постоянная R для 1 кг воздуха - в кДж/(кг∙К).
Пояснительная записка оформляется на стандартных листах А4. На на титульном листе необходимо написать название записки: «Пояснительная записка к курсовой работе по термодинамике», и далее «Расчет и анализ термодинамических циклов тепловых машин»; фамилию и инициалы студента, выполнившего работу; группу, институт и номер варианта; фамилию и инициалы преподавателя, год выполнения работы.
В конце курсовой работы студент помещает выводы, где подводит итог выполненной работы, анализирует входящие в цикл процессы, оценивает к.п.д. рассматриваемого цикла.
Дата добавления: 2021-03-18; просмотров: 53; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
