Образование углеводородов. Область применения
МИНИСТЕРСТВО НАУКИ И ВЫСШЕГО ОБРАЗОВАНИЯ РФ
ФЕДЕРАЛЬНОЕ ГОСУДАРСТВЕННОЕ БЮДЖЕТНОЕ ОБРАЗОВАТЕЛЬНОЕ УЧРЕЖДЕНИЕ ВЫСШЕГО ОБРАЗОВАНИЯ «ПЕНЗЕНСКИЙ ГОСУДАРСТВЕННЫЙ УНИВЕРСИТЕТ»
ИНСТИТУТ НЕПРЕРЫВНОГО ОБРАЗОВАНИЯ МНОГОПРОФИЛЬНЫЙ КОЛЛЕДЖ
Специальность: 40.02.02 Правоохранительная деятельность
РЕФЕРАТ
на тему:
«Углеводы(природный газ и нефть, каменный уголь) добыча и применение»
по дисциплине:
«Естествознание»
Обучающийся: Хорёнкова Артёма
Курс группа: 20КД7
Руководитель: Нестеркова Л.О
«_10_»_Декабря_2020г.
Пенза, 2020 г.
Содержание
Введение………………………………………………………………………….3
1. Классификация углеводородов………………………………………………5
3. Применение углеводородов…………………………………………………..9
2. Образование углеводородов. Область применения……………………… 10
Заключение…………………………………………………………………...…13
Введение
Углеводороды органические соединения, состоящие из атомов С (углерода) и Н (водорода) – газообразные, жидкие и твердые в зависимости от молекулярного веса и от химической структуры.
Целью реферата является рассмотрение органических соединений, на какие группы они делятся, где встречаются и возможность применения углеводородов.
Актуальность темы: Именно органическая химия является одной из наиболее быстро развивающихся химических дисциплин, всесторонне влияющих на жизнь человека. Известно, что число органических соединений слишком велико и по некоторым данным достигает порядка 18 миллионов.
Классификация углеводородов
Многочисленную группу углеводородов подразделяют на алифатические и ароматические. Алифатические, в свою очередь, делятся на две подгруппы: - насыщенные или предельные; - ненасыщенные или непредельные. В предельных углеводородах все валентности углерода использованы на соединение с соседними атомами углерода и соединение с атомами водорода. Непредельными называются углеводороды, в молекулах которых имеются атомы углерода, связанные между собой двойными или тройными связями. Классификация углеводородов систематизирована в таблице 1.
Таблица 1
Общая характеристика углеводородов
| Группа углеводородов | Степень насыщенности | Ациклические или циклические |
| Алканы | насыщенные | ациклические |
| Алкены | ненасыщенные | ациклические |
| Алкины | ненасыщенные | ациклические |
| Алкадиены | ненасыщенные | ациклические |
| Ароматические | ненасыщенные | циклические |
Алканы - это ациклические углеводороды линейного или разветвленного строения, в молекулах которых атомы углерода соединены между собой простыми s-связями. Алканы образуют гомологический ряд с общей формулой CnH2n+2, где n – число углеродных атомов.
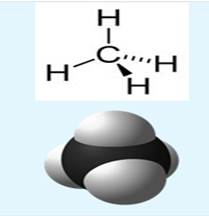
Рисунок 1. Структурная формула метана
Алкены – ациклические непредельные углеводороды линейного или разветвлённого строения, в молекуле которых имеется одна двойная связь между атомами углерода. Общая формула CnH2n.
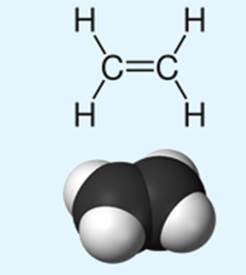
Рисунок 2. Структурная формула этилена
Алкины - непредельные ациклические углеводороды, содержащие одну тройную связь С≡С. Гомологический ряд ацетилена. Общая формула CnH2n–2. Возможна изомерия углеродного скелета, изомерия положения тройной связи, межклассовая и пространственная. Наиболее характерны реакции присоединения, горения.
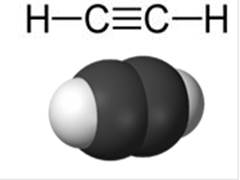
Рисунок 3. Структурная формула ацетилена
Алкадиены - непредельные ациклические углеводороды, содержащие две двойные связи С=С. Гомологический ряд диеновых углеводородов. Общая формула CnH2n–2. Возможна изомерия углеродного скелета, изомерия положения двойной связи, межклассовая, цис-транс-изомерия. Наиболее характерны реакции присоединения.

Рисунок 4. Структурная формула бутадиена-1,3
Циклоалканы - предельные карбоциклические углеводороды с одинарными связями С–С. Гомологический ряд полиметиленов. Общая формула CnH2n. Возможна изомерия углеродного скелета, пространственная, межклассовая. Для циклоалканов с n = 3–4 наиболее характерны реакции присоединения с раскрытием цикла.

Рисунок 5. Структурная формула циклопропана
ПРИРОДНЫЙ ГАЗ
В состав природного газа входит в основном метан CH4 (около 93%). Кроме метана природный газ содержит еще и другие углеводороды с короткой цепью (общая формула предельных УВ CnH2n+2), а также азот, углекислый газ, и, практически всегда, – сероводород и органические соединения нефти - меркаптаны. Именно они сообщают газу специфический неприятный запах, а при сжигании приводят к образованию токсичного диоксида серы SO2. Метан образуется при анаэробном (без доступа воздуха) сбраживании растительных и животных остатков, поэтому образуется в донных отложениях и носит название "болотного" газа.
Залежи метана в гидратированной кристаллической форме, так называемый метангидрат , обнаружены под слоем вечной мерзлоты и на больших глубинах океанов. При низких температурах (−800C) и высоких давлениях молекулы метана размещаются в пустотах кристаллической решетки водяного льда. В ледовых пустотах одного кубометра метангидрата "законсервировано" 164 кубометра газа.
НЕФТЬ
Нефть – жидкое горючее ископаемое темно-бурого цвета с плотностью 0,70 – 1,04 г/см³. Нефть представляет собой сложную смесь веществ – преимущественно жидких углеводородов. По составу нефти бывают парафиновыми, нафтеновыми и ароматическими. Однако наиболее часто встречается нефть смешанного типа. Кроме углеводородов, в состав нефти входят примеси органических кислородных и сернистых соединений, а также вода и растворенные в ней кальциевые и магниевые соли. Содержатся в нефти и механические примеси – песок и глина.
Нефть – ценное сырье для получения высококачественных видов моторного топлива. После очистки от воды и других нежелательных примесей нефть подвергают переработке. Подробно процессы технологической переработки нефти (крекинг, риформинг, платформинг) будут рассмотрены в теме "Переработка нефти"
КАМЕННЫЙ УГОЛЬ
Уголь всегда являлся перспективным сырьем для получения энергии и многих химических продуктов.
Первым крупным потребителем угля с XIX века является транспорт, затем уголь стали использовать для производства электроэнергии, металлургического кокса, получения при химической переработке разнообразных продуктов, углеграфитовых конструкционных материалов, пластических масс, горного воска, синтетического, жидкого и газообразного высококалорийного топлива, высокоазотистых кислот для производства удобрений. Методы переработки каменного угля будут также рассмотрены в теме "Методы переработки горючих ископаемых"
Назову более широкие отрасли применении углеводородов. Углеводородов в зависимости от класса много.
- в качестве топлива
- для синтеза пластмассы, резины, каучука, синтетических волокон, краски, удобрений, красителей
- для производства фармацевтических, гигиенических, косметических средств
- для производства моющих средств
- для производства пищевых добавок и пищевых продуктов
Образование углеводородов. Область применения
Основная теория происхождения углеводородов - это гниение растительных организмов и останков животных.
Используют углеводороды как топливо и как исходные продукты для синтеза разнообразных веществ. Основными источниками получения углеводородов являются природный газ и нефть.
В состав природного газа входят главным образом углеводороды с малым молекулярным весом от метана СН4 до бутана С4Н10. В состав нефти входят разнообразные углеводороды, обладающие более высоким молекулярным весом, чем углеводороды природных газов, такие как жидкие алканы С5 Н12 – С16 Н34, составляют основную массу жидких фракций нефти и твёрдые алканы состава С17 Н36 – С53 Н108 и более, которые входят в тяжёлые нефтяные фракции и твёрдые парафины.
Углеводороды, особенно циклические, получают также сухой перегонкой каменного угля и горючих сланцев.
Большое разнообразие продуктов, которые содержат в себе углеводороды, и условия, при которых они могут образоваться снова и снова, поэтому углеводороды могут играть роль профессиональных вредностей почти во всех отраслях промышленности:
ü при добыче природного жидкого и газообразного топлива (газовая, нефтедобывающая промышленность);
ü при переработке нефти и получаемых из нее продуктов (нефтеперерабатывающая и нефтехимическая промышленность);
ü при использовании продуктов термической переработки каменного и бурого угля, сланцев, торфа, нефти для самых различных целей (в качестве горючего для самолетов, автомобилей, тракторов);
ü в качестве растворителей во многих производствах, в качестве минеральных масел.
Углеводороды могут выступать как и бытовые яды:
ü при курении табака (полиароматические, такие как нафталин С10Н8 пирен С16Н10);
ü в качестве растворителей в быту (например, при чистке одежды);
ü при случайных отравлениях, главным образом детей, жидкими смесями углеводородов (бензином, керосином).
Углеводороды содержащие до 5 атомов углерода в молекуле (СН4, С2Н2, С3Н8, С4Н10, С5Н12) и представляющие собой при обычной температуре и давлении газообразные вещества, могут содержаться в воздухе в любых концентрациях и приводить в некоторых случаях к недостатку кислорода в воздухе (например, накопление СН4 в угольных шахтах) и к взрывам.
Предельные углеводороды, содержащие от 6 до 9 атомов углерода в молекуле (С6Н14, С7Н16, октан С8Н18, С9Н20), - жидкие вещества, входящие в состав бензина, керосина. Они широко применяются как растворители и разбавители клеев, лаков, красок, а также как обезжиривающие вещества и могут создавать высокие концентрации паров в производственных помещениях (резинотехническая, лакокрасочная, машиностроительная и другие отрасли промышленности).
Тяжелые углеводороды с 10 и более атомами углерода в молекуле (нефтяные и минеральные масла, парафины, нафталин, фенантрен, антрацен, битумы) отличаются малой летучестью, но вызывают те или иные поражения при хроническом воздействии на кожу и слизистые оболочки, оказывают общетоксическое действие. При работе с охлаждающими смазывающими жидкостями, например, фрезол и изготовленными на их основе эмульсолами и эмульсиями (обработка металла резанием) могут развиться масляные фолликулиты (воспалительный процесс гнойного характера).
Заключение
Рассмотрены основные классы углеводородов. Нахождение в природе и область применения.
Углеводороды нашли широкое применение в промышленности. Основная область применения:
- в качестве топлива;
- для синтеза пластмассы, резины, каучука, синтетических волокон, краски, удобрений, красителей;
- для производства фармацевтических, гигиенических, косметических средств;
- для производства моющих средств;
- для производства пищевых добавок и пищевых продуктов.
Дата добавления: 2021-02-10; просмотров: 1710; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
