Обработка экспериментальных данных.
Полученные результаты заносят в таблицу:
| Время от начала опыта, мин | Показания термометра Бекмана, град |
| 0 | ... |
| 0,5 | ... |
Для точного определения ∆T было бы идеально, если бы перед началом исследуемого процесса и по его завершении температура в калориметрическом стакане оставалась постоянной: T 1 до процесса и Т2 после него. В реальных условиях температура калориметрической системы непрерывно изменяется как до, так и после процесса вследствие теплообмена с окружающей средой. Таким образом, при определении ∆T необходимо внести поправку на теплообмен.
Весь опыт делят на три периода: 1) предварительный, продолжающийся не менее 5 минут; 2) главный — время протекания исследуемого процесса, с продолжительностью 2-3 минуты; 3) заключительный, продолжающийся также не менее 5 минут.
По экспериментальным данным строят график зависимости изменения температуры во времени (рис.2), по которому находят ∆T – изменение температуры.

Рис.2. График изиенеия температуры во времени.
Время, относящееся к участку АВ, называется начальным периодом, ВС —
главным, CD— конечным. Чтобы определить действительное изменение температуры ∆t, не искаженное тепловым обменом, происходящим в течение главного периода, продолжают линии АВ и CD до пересечения с вертикальной прямой EF , лежащей между В и С. Положение линии EF находится построением. Для этого точки т и п, соответствующие начальной и конечной температурам главного периода, наносят на ось ординат. Через середину отрезка тп проводят линию КР. Пересечение этой линии с кривой ВС дает точку l , определяющую положение прямой EF . Отрезок EF и будет действительным изменением температуры системы. Характер линии ВС зависит от условий протекания теплового процесса (например, от размешивания), наклон линий АВ и CD зависит от характера теплообмена с окружающей средой.
Таким образом, по виду кривой ABCD можно судить о качестве проведенного опыта.
На основании полученных данных вычисляют постоянную калориметра К:
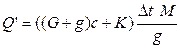 ,
,
Где Q’-молярная теплота растворения KCl(18594 Дж/моль); G-навеска воды; g-навеска KCl; c-теплоемкость раствора, принимается равной теплоемкости растворителя(4,1 кДж/град кг); M- молярная масса КСl.
Количество воды в твердом CuSO4 xH2O или соотношение количеств кристаллогидратов разных форм можно установить калориметрически. Для этого нужно знать (из таблиц) теплоты растворения безводного CuSO4 и всех форм гидратов и определить экспериментально теплоту растворения 1г исследуемого образца.
Теплоты растворения q 1г СuSO4 xH2O в 50 мл воды (кДж/г):
| СuSO4 | СuSO4 H2O | СuSO4 3H2O | СuSO4 5H2O |
| 417,0 | 219,0 | 70,9 | -46,9 |
На основании этих данных и экспериментально определенной теплоты растворения 1г исследуемой соли CuSO4.xH2O q, можно установить, какой тип равновесия существует в данном случае. Величина q зависит от того, в каком соотношении в исследуемом образце смешанны гидраты CuSO4. Если q составляет 219 - 417 кДж/г, то в системе содержится CuSO4 H2O и CuSO4. Если 71<q<219, то равновесие описывается уравнением (II) и, наконец, если q составляет от -47 до 71 кДж, то равновесие описывается уравнением (III).
Расчет теплоты растворения соли:
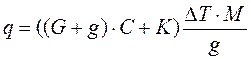 где: q – теплота растворения 1г соли, G – навеска воды, g – навеска соли, K – постоянная калориметра, ∆Т – интервал температуры(опыт), М – молярная масса CuSO4, C – теплоемкость раствора.
где: q – теплота растворения 1г соли, G – навеска воды, g – навеска соли, K – постоянная калориметра, ∆Т – интервал температуры(опыт), М – молярная масса CuSO4, C – теплоемкость раствора.
Пример расчета. Вычислить процентное содержание воды в смеси кристаллогидратов, если теплота растворения в 150 мл 3г соли составляет 240 кДж.
Вычисляем теплоту растворения 1г соли: Q=240/3=80 кДж. По данным таблицы система состоит из CuSO4 H2O и CuSO43H2O.
Решаем систему уравнений:
x+y=3,
219x+70,9y=240;
x-содержание CuSO4 H2O, а y- CuSO43H2O.
Вычисляем количество молей воды в смеси кристаллогидратов
v=3y/M(CuSO43H2O)+x/M(CuSO4 H2O).
Определяем массу воды:
g(H2O)=vM(H2O)
Определяем процентное содержание воды в соли:
γ= g(H2O)*100/m
где m – масса навески соли.
Форма отчета. Отчет должен содержать название и цель работы, краткие теоретические положения, таблицы экспериментальных данных, графики изменения температуры во времени (на миллиметровой бумаге), результаты расчета (масса воды в кристаллогидрате).
Дата добавления: 2021-02-10; просмотров: 80; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
