Тема: «Взаимодействие глюкозы и сахарозы с гидроксидом меди (II).
Номенклатура.
Сложные эфиры называют по кислотам и спиртам, остатки которых участвуют в их образовании, например Н—СО—О—СН3 — метилформиат, или метиловый эфир муравьиной кислоты; этилацетат, или этиловый эфир уксусной кислоты.
Способы получения.
1. Взаимодействие спиртов и кислот (реакция этерификации):
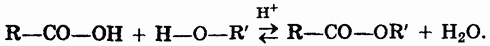
2. Взаимодействие хлорангидридов кислот и спиртов (или алкоголятов щелочных металлов):
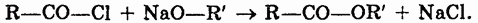
Физические свойства.
Сложные эфиры низших кислот и спиртов — жидкости легче воды, с приятным запахом. В воде растворимы только сложные эфиры с наименьшим числом атомов углерода. В спирте и диэтиловом эфире сложные эфиры растворимы хорошо.
Химические свойства.
1. Гидролиз сложных эфиров — важнейшая реакция этой группы веществ. Гидролиз под действием воды — обратимая реакция. Для смещения равновесия вправо используются щелочи:
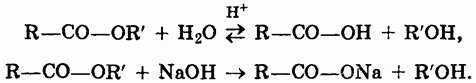
2. Восстановление сложных эфиров водородом приводит к образованию двух спиртов:
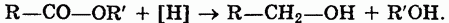
3. Под действием аммиака сложные эфиры превращаются в амиды кислот:
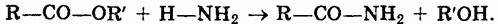
Жиры. Жиры представляют собой смеси сложных эфиров, образованных трехатомным спиртом глицерином и высшими жирными кислотами. Общая формула жиров:
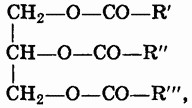
где R — радикалы высших жирных кислот.
Наиболее часто в состав жиров входят предельные кислоты пальмитиновая и стеариновая и непредельные кислоты олеиновая (С17Н33COOH) СН 3 (СН 2 ) 7 СН=СН(СН 2 ) 7 СООН и линолевая (С17Н31COOH) CH 3 (CH 2 ) 3 -(CH 2 CH=CH) 2 (CH 2 ) 7 COOH/
|
|
|
Получение жиров.
В настоящее время практическое значение имеет лишь получение жиров из природных источников животного или растительного происхождения.
Физические свойства.
Жиры, образованные предельными кислотами, — твердые вещества, а непредельными — жидкие. Все очень плохо растворимы в воде, хорошо растворимы в диэтиловом эфире.
Химические свойства.
1. Гидролиз, или омыление жиров происходит под действием воды (обратимо) или щелочей (необратимо):
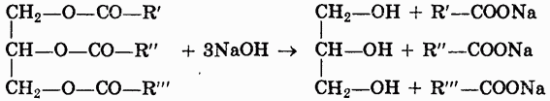
При щелочном гидролизе образуются соли высших жирных кислот, называемые мылами.
2. Гидрогенизацией жиров называется процесс присоединения водорода к остаткам непредельных кислот, входящих в состав жиров. При этом остатки непредельных кислот переходят в остатки предельных кислот, и жиры из жидких превращаются в твердые.
Из важнейших пищевых веществ — белков, жиров и углеводов — жиры обладают наибольшим запасом энергии.
ЛАБОРАТОРНАЯ РАБОТА № 13
Тема: « Доказательство непредельного характера жидкого жира»
Цель: изучить свойства жидкого жира.
Оборудование: штативы, пробирки, пробиркодержатель, спиртовки; подсолнечное масло, твердый животный жир, бромная вода
|
|
|
Ход работы:
Смотреть по ссылке: https://www.youtube.com/watch?v=YoeHAFJvho0
Опыт. Доказательства непредельного характера жидкого жира
В одну пробирку налейте 1-2 см3 подсолнечного масла, во вторую поместите кусочек твердого животного жира и нагрейте ее до расплавления жира. К содержимому каждой пробирки добавьте немного бромной воды и встряхните смеси.
Отметьте, в какой из пробирок бромная вода обесцветилась. О чем это свидетельствует?
________________________________________________________________________________
________________________________________________________________________________
________________________________________________________________________________
Составьте уравнение реакции.
________________________________________________________________________________
________________________________________________________________________________
Сделать вывод по работе:
Задание
1) Составьте уравнение реакции получения этилового эфира муравьиной кислоты.
2) Напишите уравнение реакции щелочного гидролиза тристеарата глицерина.
3) Напишите структурную формулу триглицерида, образованного одним остатком пальмитиновой кислоты и двумя остатками олеиновой кислоты.
4) Относительная плотность паров сложного эфира по водороду равна 30. Приведите структурную формулу этого эфира.
5) Имеется водный раствор, содержащий глицерин, фенол, уксусный альдегид. Как можно доказать присутствие каждого их этих веществ в растворе? Ответ обоснуйте уравнениями соответствующих химических реакций.
|
|
|
УРОК № 32 , 33 , 34
Тема: Углеводы
Смотреть по ссылке: https://www.youtube.com/watch?v=kru2Znx57dw
Углеводы – органические вещества, в которых соотношение атомов водорода и кислорода, как правило, равны 2:1.
Общая формула углеводородов: Cn (H2O)m , (n,m≥3)
Углеводы – кислородсодержащие органические вещества природного происхождения, содержащие в своем составе несколько гидроксильных групп и карбонильную группу, а также их производные.
Моносахари́ды (от греческого monos — единственный, sacchar — сахар) — простейшие углеводы, не гидролизующиеся с образованием более простых углеводов — обычно представляют собой бесцветные, легко растворимые в воде, плохо — в спирте и совсем нерастворимые в эфире, твёрдые прозрачные органические соединения, одна из основных групп углеводов, самая простая форма сахара. Водные растворы имеют нейтральную pH. Некоторые моносахариды обладают сладким вкусом. Моносахариды содержат карбонильную (альдегидную или кетонную) группу, поэтому их можно рассматривать как производные многоатомных спиртов. Моносахарид, у которого альдегидная группа расположена в конце цепи, представляет собой альдегид и называется альдоза. При любом другом положении карбонильной группы моносахарид является кетоном и называется кетоза. В зависимости от длины углеродной цепи (от трёх до десяти атомов) различают триозы, тетрозы, пентозы, гексозы, гептозы и так далее. Среди них наибольшее распространение в природе получили пентозы (5) и гексозы (6).
|
|
|
Полисахари́ды — общее название класса сложных высокомолекулярных углеводов, молекулы которых состоят из десятков, сотен или тысяч мономеров — моносахаридов.

Глюкоза и фруктоза — твердые бесцветные кристаллические вещества. Глюкоза содержится в соке винограда (отсюда название «виноградный сахар») вместе с фруктозой, которая содержится в некоторых фруктах и плодах (отсюда название «фруктовый сахар»), составляет значительную часть меда. В крови человека и животных постоянно содержится около 0,1 % глюкозы (80-120 мг в 100 мл крови). Большая ее часть (около 70 %) подвергается в тканях медленному окислению с выделением энергии и образованием конечных продуктов — углекислого газа и воды (процесс гликолиза):

ЛАБОРАТОРНАЯ РАБОТА № 14
Тема: «Взаимодействие глюкозы и сахарозы с гидроксидом меди (II).
Дата добавления: 2020-12-12; просмотров: 199; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
