Перечень кейс-заданий к государственному экзамену
1. Опишите влияние наглядных методов на качество усвоения знаний при изучения какого-либо раздела школьного курса химии
2. Опишите влияние практических методов на качество усвоения знаний какого-либо раздела школьного курса химии и приведите примеры.
3. Организуйте дидактическую игру на уроках химии.
4. Объектами исследования некоторой аналитической лаборатории являются неорганические и органические вещества, их растворы в воде и органических растворителях. Используя различные химические и физико-химические методы в лаборатории, устанавливается качественный и количественный состав анализируемых объектов. В результате количественного анализа был установлен состав неизвестного органического вещества, отвечающий формуле . 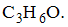 Данное вещество может относиться к гомологическим рядам…
Данное вещество может относиться к гомологическим рядам…
5. Вам выдана смесь поваренной соли, песка, железного порошка, деревянных опилок, моделирующая мусор, а также компоненты этой смеси в чистом виде. Попытайтесь найти простые и эффективные методы разделения этой смеси. Определите массовую долю каждого компонента в смеси.
6. Как вы думаете, будут ли другими методы разделения веществ, если вместо деревянных опилок в смеси присутствует медная стружка.
7. Составьте бизнес-проект по технической химии (презентацию). В Вашем распоряжении имеется сырье – известняк. Ваша задача – создать новое производство на имеющемся сырье, показать возможности создания других производств. Отразить применение, общие принципы и методы производства, схему производства (реакционный аппарат), указать химические реакции.
|
|
|
8. Вам выданы образцы воды, взятой из разных источников (они указаны на этикетках). Предположительно в них содержатся ионы: Fe2+, Fe3+, Zn2+, Cu2+, Pb2+. Составьте план их определения. Предложите способы очистки воды от этих ионов. Каковы будут ваши действия, если концентрация указанных ионов в образцах будет слишком высокой (значительно превышать ПДК)?
9. Нам известно, что соли взаимодействуют между собой при условии, что они хорошо растворимы, а в результате реакции обмена получается новая нерастворимая соль. С этих позиций получается, что взаимодействие между хлоридом железа трехвалентного и хлоридом аммония невозможно. Однако, один из способов получения азота в лабораторных условиях протекает по реакции: 6FeCl3 + 2NH4Cl = 6FeCl2 + 8HCl + N2. Налицо противоречие. Как его объяснить?
10. Вы знаете, что нерастворимые соли, например такие как (СaCO3) не должны взаимодействовать с другими солями. Однако, недавно, при проведении эксперимента в системе FeСl3+ CaCO3 мы наблюдали бурное выделение газа и выпадение бурого осадка. Для выяснения, какой это газ, мы в реакционную пробирку внесли горящую лучину, и она погасла. Мы также провели анализ осадка и выясняли, что бурые частицы осадка не растворимы в воде и щелочах, но растворимы в кислотах. Итак, вопрос: что произошло при взаимодействии FeCl3 c CaCO3, каким образом и какой газ образовался, и что из себя представляет бурый осадок?
|
|
|
На основе программы государственного экзамена составляются экзаменационные билеты, включающие вопросы, практические задания или кейс-задания, позволяющие определить уровень сформированности компетенций.
Образец экзаменационного билета
 ФГБОУ ВО
«Ульяновский
государственный
педагогический
университет
им. И.Н. Ульянова»
ФГБОУ ВО
«Ульяновский
государственный
педагогический
университет
им. И.Н. Ульянова»
| Государственный экзамен. Билет № 1. Направление подготовки 44.04.01 Педагогическое образование Направленность (профиль) образовательной программы «Химическое образование». | ||
| 1. Метрологические основы химического анализа, автоматизация анализа и использование ЭВМ в аналитической химии. 2. Реакции комплексообразования, окислительновосстановительные реакции, методы выделения, разделения и концентрирования (экстракция, хроматография, осаждение и соосаждение и др.), гравиметрический, титриметрические, кинетические, электрохимические и спектроскопические методы анализа, основные объекты анализа.
3. Практико-ориентированное задание: составьте бизнес-проект по технической химии (презентацию). В Вашем распоряжении имеется сырье – известняк. Ваша задача – создать новое производство на имеющемся сырье, показать возможности создания других производств. Отразить применение, общие принципы и методы производства, схему производства (реакционный аппарат), указать химические реакции. | |||
| Председатель ГЭК____________/ / “___” ___________ 20___ г.
| |||
Выпускная квалификационная работа демонстрирует уровень подготовленности выпускника к профессиональной деятельности.
ВКР выполняется на завершающем этапе теоретического обучения, на последнем курсе. ВКР выполняется на базе теоретических знаний и практических навыков, полученных обучающимися в период обучения, при этом подводит итог теоретического обучения обучающегося и подтверждает его профессиональные компетенции.
Тематика ВКР
1. Анализ традиционного и современного подходов к обучению химии в основной школе.
2. Влияние наглядных на качество усвоения знаний приизучения какого-либо раздела школьного курса химии
|
|
|
3. Влияние практических методов на качество усвоения знаний какого-либо раздела школьного курса химии
4. Групповые формы занятий с учащимися на уроках химии
5. Дидактические игры на уроках химии
6. Дидактические функции рабочей тетради по химии при изучении какого-либо раздела школьного курса химии
7. Использование ИКТ в школьном курсе химии
8. Использование компьютерных технологий при изучении темы «………».
9. Использование опорных схем в обучении химии
10. Использование технологии ТРИЗ на уроках химии
11. Исследовательский эксперимент на уроках химии.
12. Контроль знаний учащихся при обучении химии (анализ состояния проблемы в практике школ)
13. Методика организации на уроке самоконтроля и взаимного контроля знаний по химии
14. Методика профессиональной ориентации студентов при изучении химии в колледже
15. Методика решения экспериментальных задач по химии
16. Методические аспекты подготовки школьников к решению олимпиадных задач по химии.
17. Организация лабораторного химического практикума в школе
18. Организация проектной деятельности с учащимися по химии
19. Портфолио как средство самооценки учебных достижений школьников при обучении химии в разных классах средних образовательных учреждений.
20. Предпрофильная подготовка и профильное обучение учащихся по химии.
21. Применение технологии проектного обучения химии в школьной практике
22. Пропедевтическая подготовка учащихся по органической химии
23. Пропедевтическая подготовка учащихся по химии в VII классе
24. Развитие познавательной активности учащихся на уроках химии.
25. Разработка и использование модульного обучения химии.
26. Усиление самостоятельности учащихся как важный фактор интенсификации урока химии
27. Учебно-методический комплекс к элективному курсу «………….» в средних общеобразовательных учреждениях.
Дата добавления: 2020-04-25; просмотров: 90; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
