Алгоритм решения задачи на определение молекулярной формулы вещества по продуктам сгорания
| ПОСЛЕДОВАТЕЛЬНОСТЬ ДЕЙСТВИЙ | ПРИМЕР ВЫПОЛНЕНИЯ ДЕЙСТВИЙ |
| 1.Прочитайте текст задачи. | При сгорании 8,6 г бескислородного углеводорода образовалось 26,4 г оксида углерода (IV) и 12,6 г воды. Плотность углеводорода по воздуху равна 2,966. Определите молекулярную формулу углеводорода. |
| 2.Запишите условие и требование задачи с помощью общепринятых обозначений. | 2.Дано: m (CO2) = 26,4 г m(H2O) = 12,6 г m(вещества) = 8,6 г Dвозд. = 2,966 СхHy = ? |
| 3.Запишите уравнение реакции | 3.Решение: CxHy + O2 = CO2 + H2O |
| 4. Вычислить молярные массы веществ | Mr(CO2) = Ar(C) + 2Ar(O) = 12 + 2 · 16 = 44 M(CO2) = 44 г/моль Mr(H2O) = 2Ar(H) + Ar(O) = 2 · 1 + 16 = 18 M(H2O) = 18 г/моль |
| 5. Определим, сколько грамм углерода содержится в 26,4 г углекислого газа | 44 г CO2 содержит 12 г С
26,4 г CO2 содержит Х г С
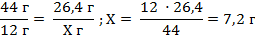
|
| 6. Определим, сколько грамм водорода содержится в 12,6 г воды | 18 г H2O содержит 2 г Н
12,6 г H2O содержит Y г H
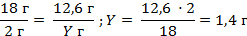
|
| 7. Находим количество вещества углерода и водорода | 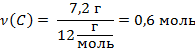
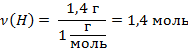
|
| 8. Составляем пропорцию | Х : Y = 0,6 : 1,4 |
| 9. Избавляемся от десятичной дроби, умножив на 10 | Х : Y = 6 : 14 |
| 10. Записать предполагаемую формулу вещества | С6H14 |
| 11. Рассчитать молярную массу предполагаемого вещества | Mr(С6H14) = 6Ar(C) + 14Ar(Н) = 6 · 12 + 14 · 1 = 86 M(С6H14) = 86 г/моль |
| 12. Рассчитать молярную массу вещества по плотности воздуха | М(вещества) = Dвозд. · 29 = 2,966 · 29 = 86 г/моль |
| 13. Сравнить полученные результаты | М(вещества) = M(С6H14) 86 г/моль = 86 г/моль |
| 14. Записать ответ | Ответ: формула вещества С6H14 |
Алгоритм определения массовой доли примесей по массе (объёму) продуктов реакции
| ПОСЛЕДОВАТЕЛЬНОСТЬ ДЕЙСТВИЙ | ПРИМЕР ВЫПОЛНЕНИЯ ДЕЙСТВИЙ |
| 1.Прочитайте текст задачи. | Определите массовую долю примесей в техническом образце карбида кальция, если из 200 г его получили 56 л ацетилена. |
| 2.Запишите условие и требование задачи с помощью общепринятых обозначений. | 2.Дано: m (CaC2) = 200 г V (C2H2) = 56 л ωпримесей = ? |
| 3.Запишите уравнение реакции | 3.Решение: CaC2 + 2Н2О = С2Н2 + Са(ОН)2 |
| 4. Пусть Х – масса чистого карбида кальция. Над формулой ацетилена запишите то, что дано в условии задачи | Х г 56 л CaC2 + 2Н2О = С2Н2 + Са(ОН)2 |
| 5. Под уравнением записываем то, что следует из уравнения реакции с учётом условий задачи (массу аммиака и объём оксида азот (П) | Mr (CaC2) = Ar(Ca) + 2Ar(C) = 40 + 2 · 12 = 64 M (CaC2) = 64 г/моль m (CaC2) = 1 моль · 64 г/моль = 64 г V (С2Н2) = ν (С2Н2) · Vm = 1 моль · 22,4 л/моль = 22,4 л Х г 56 л CaC2 + 2Н2О = С2Н2 + Са(ОН)2 64 г 22,4 л |
| 6. Составьте пропорции и определите практическую массу карбида кальция . | 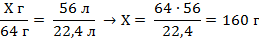
|
| 7. Определяем массу примесей | m(примесей) = 200 г – 160 г = 40 г |
| 8. Определяем массовую долю примесей | 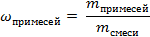
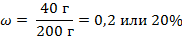
|
| 9.Запишите ответ. | Ответ: 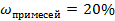
|
Алгоритм определения молекулярной формулы кристаллогидрата
| ПОСЛЕДОВАТЕЛЬНОСТЬ ДЕЙСТВИЙ | ПРИМЕР ВЫПОЛНЕНИЯ ДЕЙСТВИЙ |
| 1.Прочитайте текст задачи. | Определите формулу мирабилита, являющегося кристаллогидратом сульфата натрия, если после прокаливания навески массой 193,2 г она стала весить 85,2 г. |
| 2.Запишите условие и требование задачи с помощью общепринятых обозначений. | 2.Дано: mкристаллогидрата = 193,2 г mсоли = 85,2 г Na2SO4 · X H2O = ? |
| 3.Запишите уравнение реакции (прокаливание ведёт к испарению воды) | 3.Решение: Кристаллогидрат прокаливание сульфат натрия Na2SO4 · X H2O t0 Na2SO4 |
| 4. Над формулами записать, что известно по условию задачи | 193,2 г 85,2 г Na2SO4 · X H2O → Na2SO4 |
| 5. Под уравнением записываем то, что следует из уравнения реакции с учётом условий задачи (находим массу сульфата натрия). Масса кристаллогидрата неизвестна, принимаем за Х | Mr (Na2SO4) = 2Ar(Na) + Ar(S) + 4Ar(O) = 2 · 23 + 32 + 4 · 16 = 142 M (Na2SO4) = 142 г/моль m (Na2SO4) = 1 моль · 142 г/моль = 142 г 193,2 г 85,2 г Na2SO4 · X H2O → Na2SO4 Х г 142 г |
| 6. Составьте пропорции и определите массу кристаллогидрата . | 
|
| 7. Вычислить массу воды, которая содержится в кристаллогидрате | m(воды) = m(кристаллогидрата) - m(сульфата натрия) = 322 – 142 = 180 г Mr (H2O) = 2Ar(Н) + Ar(O) = 2 · 1 + 16 = 18 M (H2O) = 18 г/моль |
| 8. Определить количество воды в кристаллогидрате | Mr (H2O) = 2Ar(Н) + Ar(O) = 2 · 1 + 16 = 18
M (H2O) = 18 г/моль

|
| 9. Запишите ответ. | Ответ: Na2SO4 · 10 H2O |
Дата добавления: 2019-09-08; просмотров: 188; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
