Анализ адсорбции ПАВ на основе уравнения Ленгмюра
Для интерпретации адсорбции ПАВ на молекулярном уровне необходимо анализировать результаты измерений в рамках определенной теоретической модели. Параметры, получаемые при таком анализе, в дальнейшем можно использовать для сравнения адсорбционных свойств различных ПАВ и для предсказания адсорбции в новых системах. Обычно анализ адсорбции ПАВ проводят на основе уравнения Ленгмюра. Это уравнение выполняется при соблюдении следующих условий:

Рис.3. Зависимость концентрации раствора ПАВ в вытекающем из ячейки потоке от объема элюирования и соответствующая изотерма адсорбции ПАВ
1) Поверхность однородна.
2) Поверхностно-активное вещество адсорбируется с образованием одного монослоя.
3) Отсутствуют взаимодействия между молекулами ПАВ и растворителя и взаимодействия молекул ПАВ между собой.
4) Молекулы ПАВ и растворителя имеют одинаковые площади поперечного сечения.
Первые два условия вполне очевидны, а два других - нет. Было показано, что учет взаимодействий и площади поперечного сечения ПАВ приводит к нивелирующим друг друга отклонениям от уравнения Ленгмюра. Таким образом, удовлетворительное описание изотерм адсорбции ПАВ уравнением Ленгмюра в известной мере случайно. Уравнение Ленгмюра можно вывести следующим простым способом. Пусть скорость адсорбции равна

где С - равновесная концентрация ПАВ в растворе,© - доля поверхности, занятая молекулами ПАВ, ка - константа скорости. Аналогичным образом скорость десорбции записывается как
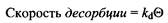
где kd - константа скорости десорбции. При равновесии скорости адсорбции и десорбции равны и тогда
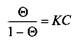 или
или
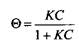
где А' - константа равновесия. Уравнения и называются уравнениями Ленгмюра. Константа равновесия К описывает распределение ПАВ между поверхностной фазой и фазой раствора.
Это становится понятным, если рассмотреть уравнение Ленгмюра при бесконечно малых концентрациях:
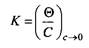
Таким образом, низкие значения К указывает на слабую адсорбцию, а высокие - на сильную адсорбцию адсорбата. Свободная энергия адсорбции GadS связана с константой К уравнением

Долю поверхности, занятую молекулами ПАВ, определяют исходя из предположение о мономолекулярной адсорбции. В этом случае полное заполнение поверхности достигается при больших равновесных концентрациях в растворе.
Доля поверхности, занятая молекулами адсорбата, определяется соотношением
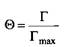
где Г - количество адсорбированного вещества, Tmax - предельная адсорбция, отвечающая полностью заполненному монослою.
Уравнение с учетом уравнения можно переписать в виде:
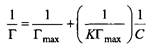
Зависимость 1/Г от 1/И позволяет определить Tmax и К по отрезку, отсекаемому на оси ординат, и по наклону прямой соответственно. Таким образом, из измеренных изотерм адсорбции определяют константы уравнения Ленгмюра Tmax и К, а также свободную энергию адсорбции AGads.
Альтернативным вариантом анализа является рассмотрение адсорбции ПАВ на твердой поверхности как его распределение между двумя фазами - поверхностной фазой и объемом раствора. При этом устанавливается равновесие между двумя фазами для молекул ПАВ и воды.
Следовательно,

Данное равновесие характеризуется константой равновесия К *
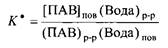
Пусть концентрация ПАВ на поверхности равна И, а концентрация воды - ; С-концентрация ПАВ в растворе, а концентрация воды в растворе постоянна из-за очень низкой концентрации ПАВ, тогда получим
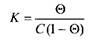
или
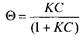
В данном анализе сделано только предположение о том, что поверхностная и объемная фазы гомогенны, что для поверхностной фазы является приближением. При более глубоком рассмотрении это предположение приводит к условиям 1-4, перечисленным ранее.
Предположением об отсутствии взаимодействий между молекулами ПАВ и растворителя можно пренебречь, если такие взаимодействия одинаковы в поверхностной и в объемной фазах. Это предположение заключено в неявной форме в приведенном выше рассмотрении, поскольку вместо активностей использованы концентрации.
Дата добавления: 2019-07-15; просмотров: 565; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
