Средства контроля концентрации и состава растворов
Содержание занятия:
Основной материал:
Контрольные вопросы
Литература
1. Кулаков М.В. Технологические измерения и приборы для химических производств. М.: Машиностроение, 2008.-423 с.
ПРАКТИЧЕСКОЕ ЗАНЯТИЕ № 8
Хроматографы
Содержание занятия:
Основной материал:
Контрольные вопросы
Литература
1. Кулаков М.В. Технологические измерения и приборы для химических производств. М.: Машиностроение, 2008.-423 с.
2. Сажин С.Г. Приборы контроля состава и качества технологических сред: Учебное пособие.- СПб.: Лань, 2012.-432 с.
ПРАКТИЧЕСКОЕ ЗАНЯТИЕ № 9
Потенциометрические анализаторы
Содержание занятия:
Основной материал:
Принцип действия основан на зависимости потенциала измерительного электрода от концентрации потенциалопределяющих ионов в растворе. Эта зависимость описывается уравнением Нернста
Понятие рН введено для линеаризации уравнения Нернста: рН (р –potencio, степень; Н –символ водорода) – равен отрицательному десятичному логарифму концентрации Н-ионов в растворе. Введя такую подстановку, можно от логарифмического уравнения перейти к линейному, алгебраическому.
Измерительный электрод (ИЭ) – это стеклянный или водородный электрод, потенциал которого зависит от концентрации Н – ионов в растворе. Электрод сравнения (ЭС) служит для контакта и замыкания цепи через исследуемый раствор (рис.6.1). Потенциал ЭС не изменяется и не зависит от концентрации Н- ионов.

Рис.6.1. Принципиальная схема рН-метра
Область применения: для автоматического контроля кислотности среды в производстве кислот, щелочей, очитке промстоков на химических предприятиях, в производстве дрожжей, аминокислот в пищевой промышленности и фармацевтике.
Устройство: в состав анализатора входит электродная ячейка и высокоомный измеритель напряжения ( потенциометр или цифровой вольтметр), имеющим токовый выход.
| Газ | 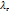 , кВт/(м , кВт/(м 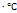 ) )
| 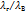
| Газ | 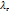 , кВт/(м , кВт/(м 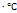 ) )
| 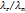
|
| Азот Аммиак Водород Воздух Двуокись азота Кислород Метан | 23,72 21,33 169,60 23,78 42,71 24,16 31,38 | 0,996 0,879 7,130 1,000 1,796 1,016 1,320 | Оксид углерода
Сернистый ангидрид
Сероводород
Углекислый газ
Хлор
Водяной пар (при100 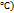
| 22,94 8,17 12,79 14,59 7,65 23,15 | 0,965 0,344 0,538 0,614 0,322 0,973 |
| Примечание | |||||
Контрольные вопросы
Литература
- Кулаков М.В. Технологические измерения и приборы для химических производств М.: Машиностроение, 2008.-424 с.
- Михайлов Б.Н., Половнева С.И., Минаева Л.В. Потенциометрические методы исследования. Учебное пособие.: Иркутск, 2002.-189 с.
ПРАКТИЧЕСКОЕ ЗАНЯТИЕ № 10
Кондуктометрические концентратомеры
Содержание занятия:
Основной материал:
Принцип действия анализатора основан на зависимости удельной электропроводности раствора от концентрации ионов.
Модель измерения : k = α*n*(U+ +U-)* C,
где
Устройство: анализатор состоит из электродной ячейки погружного или проточного типа и измерительно-преобразующего блока с дисплейным модулем. Электроды в ячейке – это металлические пластины круглой или прямоугольной формы, расположенные на строго определенном расстоянии друг от друга. Постоянная ячейки – это отношение расстояния между электродами к площади поверхности электрода: k = l/s.
Бесконтактные кондуктометры имеют в составе датчика жидкостный виток , являющийся одной из обмоток трансформатора (рис.3.1).
Контрольные вопросы
Литература
1. Кулаков М.В. Технологические измерения и приборы для химических производств. М.: Машиностроение, 2008.-423 с.
2. Сажин С.Г. Приборы контроля состава и качества технологических сред: Учебное пособие.- СПб.: Лань, 2012.-432 с.
ПРАКТИЧЕСКОЕ ЗАНЯТИЕ № 11
Оптические анализаторы
Содержание занятия:
Основной материал:
Контрольные вопросы
Литература
1. Кулаков М.В. Технологические измерения и приборы для химических производств. М.: Машиностроение, 2008.-423 с.
2. Сажин С.Г. Приборы контроля состава и качества технологических сред: Учебное пособие.- СПб.: Лань, 2012.-432 с.
ПРАКТИЧЕСКОЕ ЗАНЯТИЕ № 12
Дата добавления: 2019-03-09; просмотров: 133; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!

 - коэффициент теплопроводности соответственно газа и воздуха
- коэффициент теплопроводности соответственно газа и воздуха