Определение равновесного состава газовой смеси
Фактический состав газовой смеси Об.% : B - 50% R - 50%, что составляет их мольные доли NB ’ =0.5 NR ’ =0.5 при P общ = 1
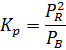
Т.к Кр>>0 = 5.01*1011, то реакция потечёт вправо, Если число молей вещ-ва увеличить B на х, то число молей вещ-ва R увеличиться на 2 x
nR = 0.5+2x; nB = 0.5-x;
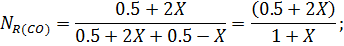
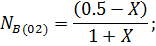

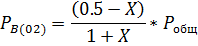
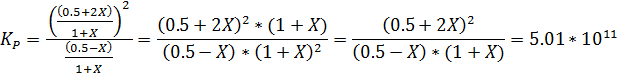
Такая ситуация возможна только в случае, если числитель стремится к нулю, т.е. либо 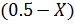 ® 0 или
® 0 или 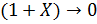
0.5-X = 0 ИЛИ 1+ X = 0
X1=0.5 X2=-1
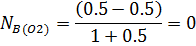
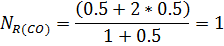
Равновесная газовая фаза состоит из одного элемента R ( CO )
Установление направления смещения равновесия
Качественно направления смещения состояния равновесия определяется принципом Ле Шателье: “если на систему, находящуюся в равновесии, оказывается воздействие, то в системе происходят такое смещение равновесия, которое ослабляет это воздействие”. Исследуемая реакция идет с выделением теплоты 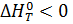 следовательно, при повышении температуры равновесие должно смещаться справа налево, так как образование исходных веществ из конечных продуктов является эндотермическим процессом и его протекание ослабляет произведенное на систему воздействие. Этот вывод согласуется с характером изменения величины Kp в зависимости от температуры (см. табл.7). Если протекание реакции сопровождается изменением числа молей газообразных продуктов (Δn ≠ 0), то давление влияет на состояние равновесия. Увеличение давления смещает равновесие в сторону веществ, занимаюших меньший обьём. В нашем случае увеличение давления смещает равновесие слева направо (∆n = -1.5), т.е. в сторону образования Оксида углерода.
следовательно, при повышении температуры равновесие должно смещаться справа налево, так как образование исходных веществ из конечных продуктов является эндотермическим процессом и его протекание ослабляет произведенное на систему воздействие. Этот вывод согласуется с характером изменения величины Kp в зависимости от температуры (см. табл.7). Если протекание реакции сопровождается изменением числа молей газообразных продуктов (Δn ≠ 0), то давление влияет на состояние равновесия. Увеличение давления смещает равновесие в сторону веществ, занимаюших меньший обьём. В нашем случае увеличение давления смещает равновесие слева направо (∆n = -1.5), т.е. в сторону образования Оксида углерода.
Дата добавления: 2019-02-26; просмотров: 102; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
