Определение перекисного окисления липидов. Общее уравнение. Особенности ПОЛ.
Переписное окисление липидов (ПОЛ) представляет собой свободнорадикальный цепной процесс, протекающий в биомембранах и липопротеинах крови, который сопровождается ступенчатой окислительной деградацией полиненасыщенных жирных кислот фосфолипидов с образованием свободнорадикальных и молекулярных продуктов, обладающих разнообразными физиологическими и патологическими эффектами.
Свободнорадикальные реакции ПОЛ постоянно протекают во всех организмах– от микроорганизмов до животных и человека.
Роль ПОЛ:
- обновление мембранных липидов
- поддержание структурного гомеостаза
- биосинтез биологически активных соединений (простагландинов, тромбоксанов, лейкотриенов)
- функционирование мембранных ферментов
- экспрессия генов
- деление клеток
- регуляция апоптоза
- Чрезмерная активация ПОЛ приводит к развитию патологических процессов (окислительный стресс).
Общее уравнение свободнорадикального ПОЛ имеет следующий вид:
(L• + LO•) + LH + O2 → (L• + LO•) + LOOH + H2O
L • , LO • - липидные радикалы
LH - полиненасыщенная жирная кислота (ПНЖК)
LOOH – гидроперекись липида
Субстратами ПОЛ являются полиненасыщенные жирные кислоты фосфолипидов, которые могут подвергаться свободнорадикальному окислению (СРО) как после гидролиза фосфолипазами типа А2, так и находясь в составе мембранных фосфолипидов. В результате ПОЛ происходит постепенная деградация ПНЖК с образованием различных свободнорадикальных интермедиатов, промежуточных высокоактивных молекулярных продуктов, а также широкого набора низкомолекулярных конечных соединений и продуктов полимеризации с неопределенной структурой.
|
|
|
Особенности:
О2 - зависимый процесс. О2 необходим для образования АКМ, для инициации процесса, реакций продолжения и разветвления цепи;
2. скорость процесса зависит не только от концентрации исходных и конечных веществ, но и от содержания промежуточных соединений – липидных радикалов;
3. большая зависимость ПОЛ от температуры среды
(Q 10 > 5);
4. скорость ПОЛ сильно зависит от степени ненасыщенности липидов;
5. ПОЛ инициируется путем отрыва атома водорода от атома углерода в α-положении, т.е. соседнего с двойной связью;
6. по типу утилизации кислорода ПОЛ относится к диоксигеназному пути окисления.
Стадии ПОЛ.
В развитии процесса ПОЛ выделяют 4 стадии:
1. Инициация или зарождение цепи. Самым мощным индуктором ПОЛ является гидроксильный радикал (ОН•).
LH + OH• → L• + H2O
Гидроксильный радикал образуется в организме в реакции Фентона:
Н2О2 + Fe2+ → ОН• + ОН▬ + Fe3+
|
|
|
2. Продолжение цепи.
L• + O2 → LO2• LO2• + LH → LOOH + L•
3. Разветвление цепи. На этой стадии участвуют металлы переменной валентности и скорость процесса возрастает в десятки раз.
LOOH + Fe2+ → LO• + OH‾ + Fe3+
4. Обрыв цепи .
L• + L• → L-L LO2• + LO2• → LOH + L=O + O2 + hῡ↑
Данная реакция называется реакцией диспропорционирования или квадратичного обрыва, в результате образуется органический спирт, кетон и высвечиваются кванты света. Эта реакция вносит важный вклад в процесс сверхслабого свечения или хемилюминесценции, который сопровождает ПОЛ.
На стадии обрыва цепи принимают участие различные антиоксиданты.
L• + InH → LH + In• ,
где InH – антиоксидант, который переходит в свободнорадикальное состояние In•, которое восстанавливается другими антиоксидантами.
Продукты ПОЛ, их характеристика.
В процессе ПОЛ образуются разнообразные продукты, которые условно делят на два типа:
1.Свободнорадикальные продукты - L•, LO•, LO2•.
2. Молекулярные продукты, которые делятся на 3 класса:
- первичные (диеновые конъюгаты, триеновые конъюгаты, диенкетоны и др.);
- вторичные, или промежуточные (карбонильные соединения – альдегиды, кетоны), в том числе малоновый диальдегид;
|
|
|
- конечные (шиффовы основания, алканы).
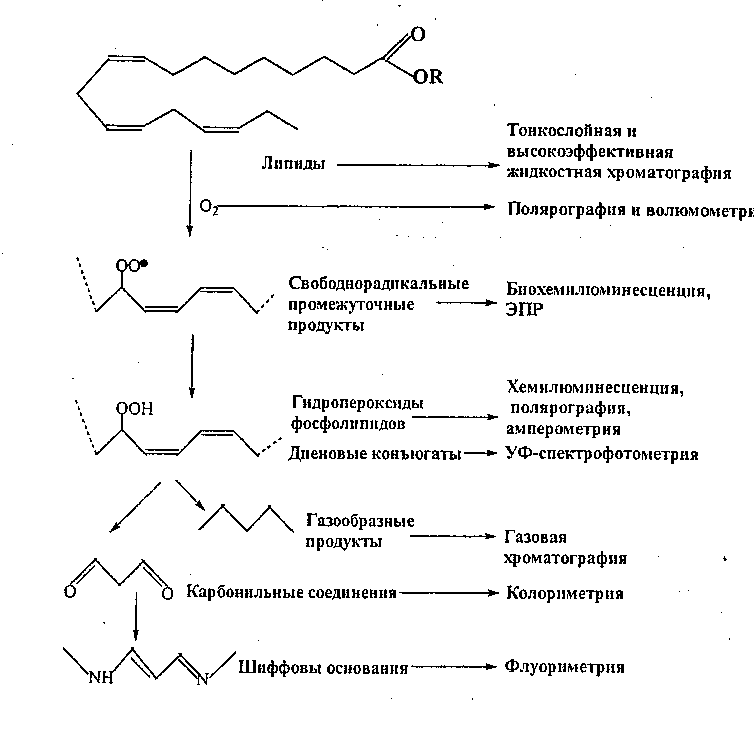
Рис.1. Продукты ПОЛ
Для поддержания ПОЛ на стационарном уровне в организме существуют антиоксидантная система, которая ингибируют ПОЛ на различных стадиях цепного процесса.
Антиоксиданты (АО) – широкий класс соединений различной химической природы, которые тормозят ПОЛ на различных стадиях цепного процесса.
К антиоксидантам относятся:
1) Ферментативные АО (супероксиддисмутаза, каталаза, пероксидазы), которые характеризуются высокой специфичностью.
Например, супероксиддисмутаза (СОД) обезвреживает супероксидный анион-радикал:
О2 ─• + О2 ─• → Н2О2 + О2
Каталаза превращает Н2О2 в воду и кислород:
2Н2О2 → 2Н2О + О2
Глутатионпероксидаза (ГПО) восстанавливает перекиси липидов до органических спиртов:
LOOH + 2GSH → LOH + GSSG + Н2О
GSH - восстановленный глутатион (Глу-Цис-Гли)
GSSG - окисленный глутатион
2) Неферментативные (низкомолекулярные) АО (аскорбат, α-токоферол, аминокислоты, пептиды, SH-соединения, эстрогены, мочевая кислота, мочевина и др.).
3) Соединения-комплексоны, которые связывают металлы переменной валентности (например, Fe2+), предотвращают реакцию Фентона, уменьшают продукцию токсичного гидроксильного радикала (ОН•) и тем самым снижают интенсивность ПОЛ (десферал, этилендиаминтетраацетат-ЭДТА).
|
|
|
4) Гидрофобные мембранотропные соединения (α-токоферол, холестерол и др.) тормозят ПОЛ в липидном бислое мембран путем восстановления активных форм кислорода и радикалов липидов (L•, LO•, LO2•).
Усиление процессов ПОЛ вследствие повышенного образования АФК и недостаточности антиоксидантной системы приводит к глубоким нарушениям структурно-функционального состояния биомембран. Это играет важную роль в механизмах окислительного стресса.
Влияние ПОЛ на биомембраны.
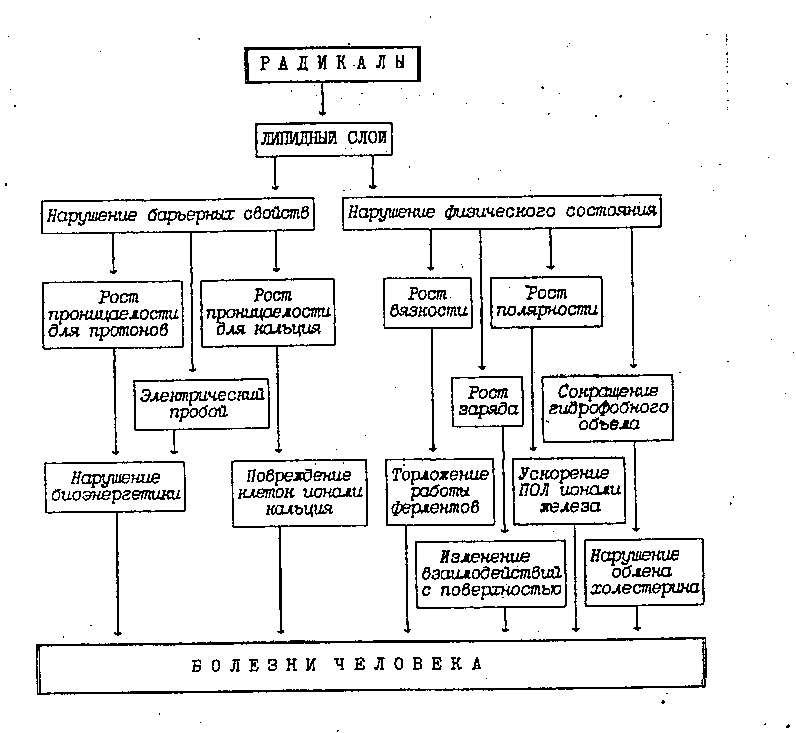
Рис. 2. Влияние ПОЛ на липидный бислой мембран
Влияние ПОЛ на липидный бислой осуществляется по 2 главным направлениям:
I. Нарушение барьерных свойств.
II. Нарушение физического состояния.
I. Нарушение барьерных свойств - это острое повреждение приводит к гибели клетки. Это повреждение реализуется путем 3 главных нарушений:
1) роста проницаемости для протонов;
2) роста проницаемости для кальция;
3) нарушения электрической стабильности мемюраны.
1.Рост проницаемости для протонов, прежде всего, наблюдается во внутренней мембране митохондрий, где локализована электрон-транспортная цепь (ЭТЦ). В норме внутренняя мембрана митохондрий не проницаема для Н+, транслокация протонов присходит через I, III, и IV ферментативные комплексы ЭТЦ против градиента концентрации за счет энергии электронов, которые поступают из цикла Кребса и переносятся по ЭТЦ. В результате повышения интенсивности ПОЛ во внутренней мембране митохондрий повышается проницаемость для протонов, что препятствует созданию ΔμН+ и последующему синтезу АТФ, что приводит к нарушению биоэнергетики.
| Комплекс I НАДН-дегидрогеназа |
| Комплекс II Сукцинат-дегидрогеназа |
| Комплекс V АТФ-синтаза |
| Комплекс IV цитохромокси-доредуктаза |
| Комплекс III Убихинон-цитохром-с-оксидоредуктаза |
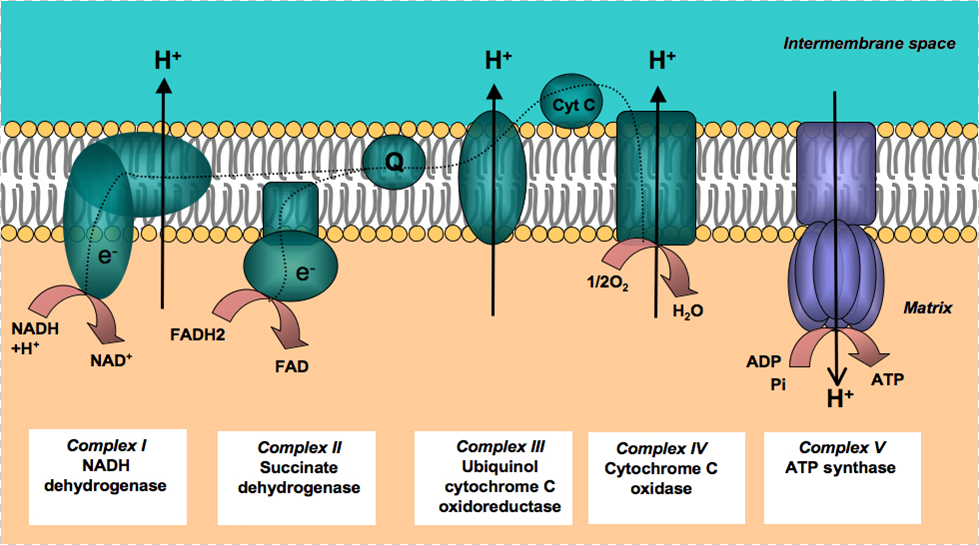
Рис.2 - Электрон-транспортная цепь митохондрий
2. Рост проницаемости для Са2+ - при активации ПОЛ происходит повышение проницаемости для кальция плазматической мембраны и субклеточных мембран: мембран ЭПР и митохондрий, где имеются депо ионов кальция. Клетка чрезвычайно чувствительна к концентрации Са2+, который является вторичным посредником и его концентрация внутри клетки в 10000 раз ниже, чем во внеклеточном пространстве. Перегрузка клетки ионами кальция может приводить к гибели клетки.
3. Электрический пробой клетки собственным мембранным потенциалом - повышение интенсивности ПОЛ приводит к нарушению электрической стабильности биомембран. Гидрофильные продукты ПОЛ типа гидроперекисей липидов (LOOH) могут выталкиваться из гидрофобного объема мембраны, что приводит к его сокращению. В результате снижается электрическая стабильность мембраны, которая может разрушаться собственным мембранным потенциалом.
II. Нарушение физического состояния биомембран - это повреждения, которые сопровождают хронические патологические процессы.
1. Рост относительной микровязкости липидного бислоя БМ - повышение интенсивности ПОЛ приводит к снижению содержания полиненасыщенных жирных кислот (ПНЖК) в мембранных липидах, т.к. ПНЖК являются субстратом ПОЛ. При протекании ПОЛ происходит ступенчатая окислительная деградация ПНЖК и насыщенность мембранных липидов увеличивается, что повышает микровязкость. Пластичность мембран снижается, они становятся более ригидными и легко разрушаются. Повышение микровязкости липидного бислоя мембран приводит к снижению активности мембранных ферментов, функция которых зависит от липидного микроокружения.
2. Рост отрицательного поверхностного заряда биомембран - при повышении уровня ПОЛ происходит образование различных продуктов ПОЛ и, прежде всего, гидроперекисей липидов, которые гидрофильны и вследствие гидрофобности внутреннего объема мембраны могут изменять свою локализацию.
Диффузия к поверхности раздела мембраны гидрофильное/гидрофобное - на границе с цитоплазмой или внеклеточной средой. Здесь на границе раздела гидроперекиси липидов диссоциируют: LOOH ↔ H+ + LOO-. Анионы гидроперекисей липидов вызывают повышение отрицательного поверхностного заряда биомембран, что негативно влияет на межклеточные взаимодействия.
3. Рост полярности гидрофобного объема мембраны - при усилении ПОЛ во внутреннем пространстве мембраны образуются гидрофильные продукты ПОЛ (гидроперекиси и др.), которые в силу гидрофобности внутреннего объема образуют "гидрофильные кластеры" для уменьшения контактов с гидрофобным микроокружением. В гидрофильные кластеры устремляются различные гидрофильные молекулы, в том числе, вода и Fe2+. Диффузия воды во внутренний объем мембраны нарушает ее стабильность. Это явление Владимиров Ю.А. назвал "водной коррозией" мембраны.
Появление Fe2+ в гидрофильных кластерах мембраны приводит к запуску реакции разветвления цепи c образованием высоко токсичного липоксильного радикала и еще большему усилению ПОЛ:
LOOH + Fe2+ ↔ LO● + OH─ + Fe3+
4. Сокращение гидрофобного объема мембраны - в результате усиления ПОЛ часть гидрофильных продуктов ПОЛ выталкиваются из мембраны, что приводит к снижению гидрофобного объема мембраны. Это приводит к нарушению обмена холестерина. В результате ПОЛ и изменения структуры липопротеинов низкой плотности (ЛПНП), которые являются транспортной формой холестерина в крови, ЛПНП легче отдают холестерин, например, мембранам клеток крови, а липопротеины высокой плотности значительно медленнее забирают холестерин из мембран. В результате холестерин накапливается в мембранах и повышает их микровязкость. Известно, что микровязкость липидного бислоя повышается при увеличении содержания ПНЖК и холестерина.
5. Скрамблинг - нарушение асимметрии липидного бислоя мембран. Известно, что важнейшим свойством мембранных липидов является трансмембранная асимметрия липидного бислоя, т.е. различное распределение липидов между внутренним и наружным монослоями.
1. Во внешнем монослое локализуются холинсодержащие ФЛ (фосфатидилхолин, сфингомиелин), а также стероид холестерол.
2. Во внутреннем монослое локализуются аминосодержащие ФЛ (фосфатидилэтаноламин, фосфатидилсерин).
3. Во внешнем монослое сосредоточена 1/3 двойных связей, во внутреннем – 2/3 двойных связей.
При усилении ПОЛ активируются скрамблазы, которые нарушают асимметрию липидного бислоя. В результате во внешнем монослое появляется фосфатидилсерин (ФС), который называют рецептором "съешь меня". Он является сигналом к апоптозу и поглощению клетки макрофагами.
Понятие об антиоксидантах.
См продукты 28
Доп
Для поддержания активности процессов ПОЛ на стационарном уровне в организме, имеются разнообразные антиоксидантные системы. Недостаток поступления облигатных антиоксидантов и дефицит эндогенных антиоксидантных систем приводит к развитию свободно-радикальных патологий. Действие внешних прооксидантов (радиация, ультрафиолет; загрязнители воздуха, гипероксия, гипоксия и др.) и активация эндогенных механизмов генерации активированных кислородных метаболитов (АКМ) приводит к напряжению механизмов антиоксидантной защиты и развитию окислительного стресса, при котором происходит сдвиг равновесия системы антиоксиданты прооксиданты в сторону последних. Окислительный стресс играет важную роль в патогенезе многих заболеваний.
В инициации ПОЛ ведущая роль отводится активным формам кислорода (АФК), которые постоянно образуются в организме:
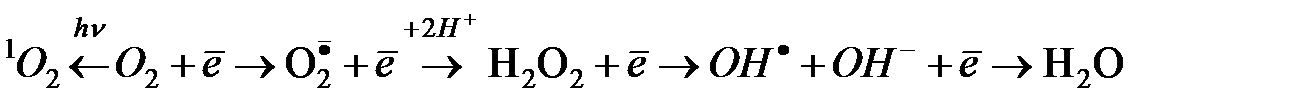
Процесс последовательного восстановлении кислорода лежит в основе двух главных типов окислительных превращений биосубстратрв в клетке: оксидазного и оксигеназного.

Схема участия молекулярного кислорода в окислительных превращениях субстратов (S) в клетке.
Типичным примером оксидазного пути являются процессы окисления энергетических субстратов в митохондриях, где восстановление кислорода катализируется цитохромоксидазой. Огромное разнообразие реакций гидроксилирования монооксигеназного типа в клетках катализируется полиферментным комплексом, содержащим в качестве терминальной оксигеназы цитохром Р-450.
Примером реакции диоксигеназного типа является процесс перекисного окисления внутриклеточных липидных субстрато
Дата добавления: 2019-02-22; просмотров: 2898; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
