Соединительная ткань со специальными свойствами
Слизистая соединительная ткань – тип рыхлой соединительной ткани, наблюдается у эмбриона (в глубоких слоях кожи и пупочном канатике). Содержит крупные звездообразные фибробласты и желеобразное основное вещество с некоторым количеством коллагеновых волокон.
Эмбриональная соединительная ткань состоит из звездчатых, бледно окрашивающихся мезенхимных клеток, погруженных в гелеобразное аморфное основное вещество, содержащее небольшое количество широко разбросанных волокон (в основном ретикулярных). В этих полипотентных мезенхимных клетках часто наблюдаются фигуры митоза.
Ретикулярная соединительная ткань – пучки тонких, мелких коллагеновых волокон, которые окрашиваются в черный цвет нитратом серебра. Расположена вокруг синусоидов печени и формирует строму лимфатических органов. Кроме ретикулярных клеток, имеет много блуждающих клеток (лейкоциты, макрофаги и т. п.).
Жировая соединительная ткань может быть белой (однокамерной) или бурой (многокамерной).
Белая жировая ткань запасает жир в крупных жировых клетках, разделяется на доли и дольки тонкими листками фиброзной соединительной ткани; богато васкуляризована и иннервирована.
Бурая жировая ткань состоит из многокамерных адипоцитов, которые содержат многочисленные митохондрии; имеется в основном у новорожденных и животных, впадающих в спячку. Также хорошо кровоснабжается и иннервируется.
Функция: выделяет тепло, разобщая клеточное дыхание и окислительное фосфорилирование.
Тесты и вопросы для самоконтроля
1. На гистологическом препарате рядом с тканевыми базофилами видно большое количество гранул. Какие вещества выделились из клеток и как называется этот процесс?
2. Вокруг капилляров располагаются клетки с базофильной зернистостью. Как называются эти клетки, что они выделяют и каково их влияние на функциональное состояние капилляров?
3. Известно, что кровяные пластинки (тромбоциты) принимают участие в процессе свертывания крови. Какие клетки соединительной ткани препятствуют этому?
4. Под влиянием ультрафиолетовых лучей изменился цвет кожи. Какие клетки соединительной ткани принимают участие в этой реакции?
5. У больного в межклеточном веществе увеличено количество гликозаминогликанов. Какие клетки соединительной ткани принимают участие в этом процессе?
6. Под кожу попало инородное тело. Какова будет реакция рыхлой соединительной ткани и какие клетки в ней участвуют?
7. У человека при авитаминозе в фибробластах рыхлой волокнистой соединительной ткани нарушен синтез белка тропоколлагена. Какие изменения будут отмечены в межклеточном веществе?
8. В рыхлой волокнистой соединительной ткани нарушено образование основного вещества. Нарушением функций каких основных клеток может быть вызвано это явление?
9. При использовании светового микроскопа на препарате рыхлой волокнистой соединительной ткани видны овальные клетки средних размеров, с круглым ядром, хроматин в котором расположен в виде колесика со спицами. На электронограмме видна очень хорошо развитая гранулярная цитоплазматическая сеть. Как называются эти клетки?
10. В месте внедрения инородного тела в организме возникает воспаление с участием клеток крови и рыхлой волокнистой соединительной ткани. Какие клетки крови и соединительной ткани будут обнаружены в очаге воспаления?
11. На препарате видны овальные клетки в виде пустых ячеек с уплощенным ядром, расположенным вблизи клеточной мембраны. Какие это клетки и что они образуют?
12. При исследовании соединительной ткани видна клетка с хорошо выраженной специфической базофильной зернистостью. Как называется эта клетка?
13. Известно, что клетки рыхлой волокнистой соединительной ткани имеют различный генез. В условном эксперименте в период гисто‑и органогенеза разрушено развитие клеток, производных мезенхимы. Нарушение развития каких клеток рыхлой волокнистой соединительной ткани будет наблюдаться при этом?
14. Гигантские клетки чужеродных тел – это объединение: а) макрофагов, б) лимфоцитов, в) фибробластов, г) адипоцитов.
Ответы
1. Серотонин, гистамин; дегрануляция.
2. Тканевые базофилы; гистамин, выделяемый этими клетками, способствует расширению капилляров и увеличению проницаемости их стенок.
3. Тканевые базофилы, эндотелиоциты.
4. Пигментные клетки.
5. Фибробласты, тканевые базофилы.
6. Воспалительная; нейтрофилы, макрофаги, фибробласты.
7. Нарушается процесс формирования коллагеновых волокон.
8. Фибробластов, фиброцитов, тканевых базофилов.
9. Плазматические клетки.
10. Нейтрофилы, лимфоциты, макрофаги, фибробласты.
11. Жировые клетки, жир.
12. Тканевой базофил.
13. Фибробластов.
14: а) гигантские клетки чужеродных тел образуются при слиянии макрофагов.
Глава 5
Кровь и кроветворение
Кровь
Кровь – особый тип соединительной ткани, который состоит из форменных элементов (клетки и кровяные пластинки), взвешенных в жидком межклеточном веществе (плазма).
Средний объем крови в организме взрослого человека около 5 л, что составляет 6–8 % от массы тела.
Кровь циркулирует по всему телу по замкнутой системе сосудов, доставляя к органам и тканям различные питательные вещества, газы (кислород, углекислый газ), гормоны, белки, электролиты и т. д. В этом проявляется ее транспортная функция:
– регулирует температуру тела (терморегуляторная функция) и участвует в регуляции осмотического и кислотно‑основного равновесия (гомеостатическая функция);
– удаляет из тканей продукты метаболизма и выделяет их с мочой из организма (экскреторная функция);
– нейтрализует чужеродные антигены, обезвреживает микроорганизмы за счет неспецифических и специфических (иммунных) механизмов (защитная функция).
Циркулирующие форменные элементы крови имеют относительно небольшую продолжительность жизни, поэтому они должны постоянно заменяться. Процесс образования новых форменных элементов называется гемоцитопоэзом.
Плазма крови
В плазме 90 % воды, 9 % органических компонентов (белки, аминокислоты и т. д.) и 1 % неорганических солей.
Белки плазмы – это фибриноген, альбумины, глобулины, компоненты комплемента, обеспечивающие ее вязкость, онкотическое давление, свертываемость, перенос различных веществ и защитные функции.
Фибриноген переходит в фибрин под действием различных белков – ферментов крови и кофакторов, обеспечивая свертывание крови.
Альбумины – белки небольшой молекулярной массы (60 000), количественно преобладающие в плазме крови; их функция – поддержание осмотического давления в сосудистой системе и транспорт определенных метаболитов.
Глобулины бывают трех типов: α, β и γ:
– γ‑глобулины – это антитела, утилизируемые в ходе реакций иммунологической защиты;
– α– и β‑глобулины транспортируют ионы металлов (железо и медь) и липиды (в форме липопротеинов).
Компоненты комплемента участвуют в неспецифических защитных реакциях.
Сыворотка крови – жидкость, остающаяся после свертывания крови, в которой отсутствует фибриноген и факторы свертывания.
Форменные элементы крови
Эритроцит (erythrocytus) – это круглый двояковогнутый диск (дискоцит); окрашивается в светлый оранжево‑розовый цвет при окраске по методу Романовского – Гимзы. Зрелые эритроциты не имеют ядер.
Дискоциты составляют 90 % от всех зрелых эритроцитов, остальные – это сфероциты и эхиноциты.
Диаметр эритроцитов 7,16–7,98 мкм (75 % всех эритроцитов – это нормоциты), но может уменьшаться до 6 мкм и менее (12,5 % – это микроциты) или увеличиваться до 8,5–9,0 мкм (12,5 % – это макроциты).
Ультраструктура: в зрелом эритроците нет ни органелл, ни ядра; в нем 60 % воды и 40 % – сухой остаток, в основном гемоглобин и периферические белки.
Гемоглобин состоит из четырех полипептидных цепочек, каждая ковалентно связана с гемом (модифицированное порфириновое кольцо).
Типы нормального гемоглобина взрослого человека зависят от последовательности аминокислотных остатков в полипептидных цепях и известны как HbA1, HbA и HbF (гемоглобин плода); преобладает HbA. Иногда в популяции встречается атипичный гемоглобин S (HbS), являющийся результатом точечных мутационных процессов.
Периферические белки связаны с внутренней стороной клеточной мембраны. Наибольшее значение имеют протеин 4,1, анкирин, спектрин, гликофорин и актин.
Спектрин и актин помогают поддерживать форму зрелого эритроцита, в то время как протеин 4,1 и анкирин связывают актин и спектрин с интегральными белками на поверхности плазматической мембраны.
Количество эритроцитов в 1 мкл 3,9–5,5 106 у мужчин и 3,7–4,7 106 у женщин (соответственно 3,9–5,5 1012/л и 3,7–4,7 • 1012/л).
Продолжительность жизни: при циркуляции примерно 100–200 дней (в среднем 120 дней), а затем разрушаются макрофагами селезенки и в меньшей степени печени и красного костного мозга.
Функция эритроцитов : транспорт кислорода в ткани тела и двуоксида углерода из них:
– в областях высокого парциального давления кислорода (в легких) гемоглобин избирательно присоединяет кислород, формируя оксигемоглобин;
– в областях высокого парциального давления двуоксида углерода (в тканях) оксигемоглобин освобождает кислород, обменивая его на двуоксид углерода, формируя карбоксигемоглобин;
– перенос на своей поверхности некоторых гормонов (инсулин) и ядов (оксид углерода), ряда биологически активных веществ (иммуноглобулины, компоненты комплемента, иммунные комплексы).
Лейкоцит (leukocytus) – форменный элемент крови, имеющий ядро. Выделяют две группы лейкоцитов: гранулоциты и агранулоциты в зависимости от наличия или отсутствия в их цитоплазме специфических гранул.
В 1 мкл крови количество лейкоцитов составляет от 4000 до 9000 (4–9 109/л).
К гранулоцитам относятся нейтрофильные гранулоциты (нейтрофилы), эозинофильные гранулоциты (эозинофилы) и базофильные гранулоциты (базофилы), к агранулоцитам – моноциты и лимфоциты.
Нейтрофильный гранулоцит (granulocytus neutrophilicus), или нейтрофил (рис. 5.1), – это округлая клетка диаметром 9–12 мкм с темно‑синим сегментированным ядром (обычно 3–4 сегмента), сегменты которого соединены тонкими перемычками хроматина. В нейтрофилах женщин определяется тельце Барра (половая хромосома) – выпячивание ядра в виде барабанной палочки. Это находящаяся в неактивной форме одна из двух Х‑хромосом.

Рис. 5.1. Нейтрофильный гранулоцит. ТЭМ. ×10 000.
1 – сегменты ядра; 2 – азурофильные гранулы; 3 – специфические гранулы; 4 – псевдоподия.
Ультраструктура: небольшой, центрально расположенный комплекс Гольджи, редкая гранулярная эндоплазматическая сеть, небольшое количество митохондрий и свободных рибосом.
В цитоплазме находятся специфические гранулы, первичные лизосомы в виде азурофильных гранул и некоторое количество гликогена.
Специфические, или вторичные, гранулы окрашиваются слабо. Это мелкие (диаметром 100–300 нм), как правило, сферические образования, окруженные однослойной мембраной.
Содержимое гранул: лизоцим, фагоцитин, коллагеназа, щелочная фосфатаза, лактоферрин, активатор плазминогена, а также адгезивные белки.
Азурофильные гранулы (первичные лизосомы) значительно крупнее (диаметром примерно 0,5 мкм), чем специфические, их меньше.
Они содержат различные гидролитические ферменты, участвующие в фагоцитозе, а также лизоцим, миелопероксидазу, нейтральные протеазы, дефензины, катионные антимикробные белки, бактерицидный белок, увеличивающий проницаемость.
Третичные гранулы содержат желатиназу, лизоцим, адгезивные белки и другие ферменты.
Секреторные пузырьки несут на своих мембранах большое количество адгезивных белков и рецепторов хемотаксических факторов.
Количество: в 1 мкл от 3500 до 7000 (65–75 % от всех лейкоцитов).
Продолжительность жизни около недели (6–7 дней).
Функция: прежде всего защитная (фагоцитарная). Эти клетки мигрируют из кровотока между эндотелиальными клетками стенок сосудов микроциркуляторного русла путем диапедеза в пространства соединительной ткани, чтобы сформировать первую линию защиты:
– опознают и фагоцитируют бактерии, образуя фагосомы;
– специфические гранулы затем сливаются с фагосомами, обеспечивая переваривание их содержимого;
– азурофильные гранулы также сливаются с фагосомами, выделяя в них свои гидролитические ферменты, переваривая микроорганизмы и часто убивая саму клетку.
Гной – это скопление мертвых нейтрофилов, макрофагов, микроорганизмов и тканевой жидкости.
Нейтрофилы участвуют в регуляции деятельности других клеток, вырабатывая ряд цитокинов.
Третичные гранулы участвуют в переваривании субстратов в межклеточном пространстве, в процессах адгезии и, возможно, фагоцитоза.
Секреторные пузырьки, сливаясь с плазмолеммой, обеспечивают приток адгезивных молекул, необходимых для формирования прочной связи нейтрофила с эндотелием сосуда.
Эозинофильный (ацидофильный) гранулоцит (granulocytus eosinophilicum), или эозинофил, – это округлая клетка диаметром 10–14 мкм. Ядро темное, чаще двудольное, напоминающее пару связанных сосисок.
Цитоплазма непрозрачна из‑за множества специфических гранул, окрашивающихся в красновато‑оранжевый цвет. Присутствуют также азурофильные гранулы (первичные лизосомы) и, редко, микрогранулы.
Ультраструктура: органеллы относительно немногочисленные, множество митохондрий, комплекс Гольджи и гранулярная эндоплазматическая сеть, а также значительные запасы гликогена.
Специфические гранулы! – крупные эллипсощцше образования длиной 0,5–1,5 мкм и шириной 0,3–1,0 мкм, окруженные однослойной мембраной. На электронных микрофотографиях выявляется наличие в гранулах вытянутой кристалловидной сердцевины, окруженной хлопьевидным и гомогенным веществом.
Содержат лизосомальные ферменты, катионный белок, нейротоксин, гистаминазу, пероксидазу и главный основной белок (богатый аргинином) – компонент кристалловидной сердцевины, который инактивирует гистамин, гепарин и простагландины, а также оказывает антигельминтное, антипротозойное и антибактериальное действие.
Азурофильные гранулы! (первичные лизосомы) диаметром 0,5 мкм находятся в цитоплазме в небольшом количестве. Они содержат кислую фосфатазу, арилсульфатазу и другие гидролитические ферменты.
Количество в 1 мкл 150–400 (от 1 до 5 % от всех лейкоцитов).
Продолжительность жизни 6–8 дней, в кровеносном русле находятся всего 3–8 ч, поэтому основная часть эозинофилов содержится в периферических тканях (на один эозинофил в крови приходится 100–300 эозинофилов в тканях).
Функция до конца не выяснена. Считают, что эозинофилы фагоцитируют комплексы антиген – антитело, а также связаны с инактивированием и уничтожением паразитарных факторов (гельминтов и простейших) нефагоцитарным механизмом;
– они также инактивируют гистамин и лейкотриены, которые выделяются тканевыми базофилами (тучными клетками) и базофильными гранулоцитами;
– аллергические реакции вызывают увеличение популяции эозинофилов, что косвенно указывает на их участие в этих процессах.
Базофильный гранулоцит (granulocytus basophilicus), или базофил, – это округлая клетка диаметром 8–10 мкм. Имеет светло‑синее S‑образное ядро, часто замаскированное многочисленными темными крупными специфическими гранулами. Присутствуют также азурофильные гранулы.
Ультраструктура: органеллы сравнительно немногочисленные, хотя присутствуют митохондрии, комплекс Гольджи и гранулярная эндоплазматическая сеть;
– цитоплазма содержит специфические гранулы, небольшое количество гликогена, липидные капли и азурофильные гранулы.
Специфические гранулы крупные (диаметр 0,5–1,3 мкм), ограниченные мембраной сферические структуры, содержащие гранулярные частицы в гомогенно‑хлопьевидном основном веществе;
– содержат гепарин, гистамин, пероксидазу, ферменты (протеазы и др.), хемотаксические факторы эозинофилов и нейтрофилов и, вероятно, анафилактический фактор.
Азурофильные гранулы (первичные лизосомы) немногочисленные, содержат гидролитические ферменты.
Количество: это самые малочисленные из всех клеток крови, от 50 до 100 в 1 мкл (0,5–1 % от всех лейкоцитов).
Продолжительность жизни, вероятно, большая (например, у мыши от 1 до 1,5 года); у человека предположительно до нескольких суток.
Функция: подобно тучным клеткам базофилы выделяют гистамин, гепарин, анафилактический фактор и эозинофильный хемотаксический фактор (регуляторная и защитная функции). Обладают слабой фагоцитарной активностью.
Моноцит (monocytus) – самая крупная из всех циркулирующих клеток, диаметром от 12 до 15 мкм.
Ядро ацентрическое, бобовидное или подковообразное (реже дольчатое), имеет выраженную сеть глыбок гетерохроматина. Присутствуют обычно 1–2 ядрышка.
Цитоплазма серо‑голубая, содержащая многочисленные азурофильные гранулы. Специфические гранулы отсутствуют.
Ультраструктура: комплекс Гольджи, относительно редкая гранулярная эндоплазматическая сеть, небольшое количество митохондрий и рибосом. Присутствуют также азурофильные гранулы, гликоген, микрофиламенты и микротрубочки. Отмечается наличие цитоподий, пиноцитозных пузырьков, фагосом.
Азурофильные гранулы очень многочисленные. Это первичные лизосомы (диаметр 0,5 мкм), содержащие, кроме других ферментов, пероксидазу, лизоцим, лактоферрин, катионные белки, миелопероксидазу, перекись водорода и другие биоокислители, кислую фосфатазу и арилсульфатазу.
Количество: в 1 мкл от 200 до 800 (6–8 % всех лейкоцитов).
Продолжительность жизни: в кровеносном русле, вероятно, менее 3 дней, в тканях – от 40 до 60 дней.
Функция: моноциты мигрируют в соединительную ткань, где дифференцируются в макрофаги и фагоцитируют чужеродные агенты и вещества;
– влияют на иммунные процессы, способствуя продукции антител иммунокомпетентными клетками (плазмоцитами);
– осуществляют захват и внутриклеточное переваривание различных стареющих и погибших клеток и постклеточных структур (в том числе форменных элементов крови), а также их фрагментов;
– секретирует различные вещества, регулирующие состояние межклеточного вещества (лизосомальные протеазы, коллагеназы, эластазы и др.) и функциональную активность и пролиферацию клеток других типов (монокины).
Лимфоцит (lymphocytus) – это сферическая мелкая клетка диаметром 8–10 мкм; окрашенное ядро занимает большую часть клетки, оставляя узкий ободок светлой голубой цитоплазмы на периферии (рис. 5.2).
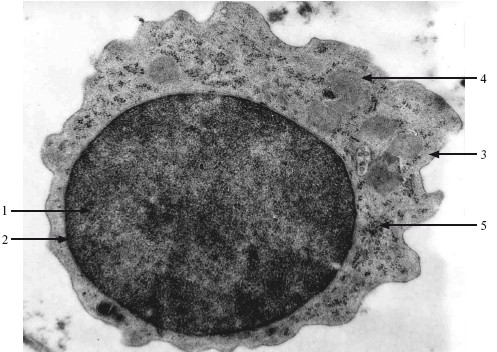
Рис. 5.2. Лимфоцит. ТЭМ. ×18 000.
1 – ядро; 2 – гетерохроматин; 3 – цитоплазма; 4 – митохондрия; 5 – рибосомы.
Ультраструктура: небольшое количество митохондрий, слаборазвитый комплекс Гольджи, почти нет гранулярной эндоплазматической сети, но большое количество свободных рибосом. Присутствует также некоторое количество лизосом (азурофильные гранулы диаметром 0,5 мкм).
Лимфоциты – единственные клетки крови, способные при определенных условиях митотически делиться.
Лимфоциты – весьма гетерогенная (неоднородная) популяция клеток.
Классификация лимфоцитов: 1) по размерам и морфологии; 2) по генезису (особенностям развития); 3) по функции; 4) по рецепторам к антигенам; 5) по продолжительности жизни.
По размерам лимфоциты подразделяются на малые – 4,5–6 мкм; средние – 7–10 мкм и большие – более 10 мкм.
В крови около 90 % малых (зрелые) и 10–12 % средних лимфоцитов. Большие (бластные) лимфоциты в нормальных условиях в крови не встречаются.
В крови взрослого человека наблюдаются также большие гранулярные лимфоциты (5–10 % от всех лимфоцитов крови) с бобовидным асимметрическим ядром и цитоплазмой, содержащей крупные азурофильные гранулы с перфорином и гранзимами, обеспечивающими цитотоксическую активность этих клеток. Они выполняют функцию NK‑клеток, или естественных киллеров, – особой разновидности эффекторных клеток иммунной системы.
По особенностям ультраструктуры малые лимфоциты подразделяются на светлые (70–75 %) и темные (12–13 %). По источникам развития выделяют:
– Т‑лимфоциты: их образование и дальнейшее развитие связано с тимусом;
– В‑лимфоциты: их развитие у птиц связано со специальным органом в области задней кишки – фабрициевой сумкой, а у млекопитающих и человека – пока точно не установленным ее аналогом (скорее всего, с красным костным мозгом).
По функции:
I. Т‑лимфоциты, обеспечивающие клеточный, или врожденный, иммунитет, подразделяют на субпопуляции: 1) киллеры, 2) хелперы, 3) супрессоры, 4) клетки памяти, 5) амплифайеры, 6) дифференцирующие и др.;
– Т‑киллеры, или цитотоксические лимфоциты, обеспечивают защиту организма от чужеродных клеток или генетически измененных собственных клеток;
– Т‑хелперы регулируют гуморальный иммунитет, усиливая деятельность В‑лимфоцитов;
– Т‑супрессоры также участвуют в регуляции гуморального иммунитета, угнетая функцию плазмоцитов;
– Т‑клетки памяти: короткоживущие (месяцы) и долгоживущие (годы);
– Т‑амплифайеры (усилители) усиливают функции Т‑киллеров, хелперов, супрессоров и других иммунокомпетентных клеток;
– Т‑дифференцирующие клетки оказывают влияние на пролиферацию и дифференцировку стволовых клеток.
II. В‑лимфоциты, обеспечивающие гуморальный, или приобретенный, иммунитет;
– защиту организма от чужеродных корпускулярных антигенов: бактерий, вирусов, токсинов, белков и др. Среди В‑лимфоцитов выделяют:
– рецепторные (нулевые) В‑лимфоциты, которые выполняют только рецепторные функции, т. е. распознают соответствующий их рецепторам антиген;
– эффекторные В‑лимфоциты (плазмоциты), трансформирующиеся из «нулевых» клеток под влиянием антигена в присутствии Т‑хелперов и макрофагов и активно продуцирующие антитела;
– В‑клетки памяти: короткоживущие (недели) и долгоживущие (месяцы).
В пределах своих субпопуляций Т– и В‑лимфоциты различаются между собой по типам рецепторов к разным антигенам, образуя группы (клоны) клеток, имеющие одинаковые рецепторы. При встрече лимфоцита с антигеном, к которому у него есть рецептор, лимфоцит стимулируется, превращается в лимфобласт, а затем пролиферирует и дифференцируется, в результате чего образуется клон новых лимфоцитов с одинаковыми рецепторами.
Количество: это вторая по многочисленности популяция агранулоцитов крови – в 1 мкл от 1500 до 2500 (20–25 % от всех лейкоцитов).
Продолжительность жизни: Т‑лимфоциты могут жить несколько лет, В‑лимфоциты погибают через несколько месяцев.
Функция: Т‑лимфоциты ответственны в первую очередь за клеточный (врожденный) иммунитет, В‑лимфоциты обеспечивают гуморальный (приобретенный) иммунитет.
Тромбоцит (thrombocytus), или кровяная пластинка, – это округлый или овальный фрагмент клетки диаметром 2–4 мкм. Тромбоциты происходят от мегакариоцитов в красном костном мозге.
Кровяные пластинки имеют прозрачный периферический участок (гиаломер) и более плотный гранулярный центр (грануломер).
Гиаломер содержит актиновые микрофиламенты цитоскелета и микротрубочки, а также промежуточные филаменты; систему трубочек, соединенную с поверхностью (открытая система канальцев), обеспечивающую экзоцитоз содержимого гранул тромбоцитов, и плотную систему трубочек (которая, вероятно, накапливает и выделяет ионы кальция, а также вырабатывает простагландины);
– микротрубочки (4–15) формируют краевое кольцо по периферии цитоплазмы, служащее для поддержания формы тромбоцита;
– промежуточные филаменты образованы белком виментином.
Грануломер состоит из α‑гранул (диаметр от 300 до 500 нм), плотных телец, или 5‑гранул (диаметр от 250 до 300 нм), 1‑гранул, редко встречающихся митохондрий, некоторого количества лизосом и частиц гликогена;
– плазмолемму покрывает гликокаликс, состоящий из гликозаминогликанов и гликопротеинов. В присутствии ионов кальция и АДФ он способствует слипанию кровяных пластинок, так что в случае необходимости они могут приклеиваться друг к другу и к стенке сосуда;
– α‑гранулы содержат фибриноген, фибронектин, тромбопластин кровяных пластинок, тромбоцитарный фактор роста, тромбоглобулин, тромбоспондин и фактор свертывания V;
– плотные тельца (с плотным матриксом) содержат АДФ, АТФ, ионы кальция, магния, пирофосфат, гистамин, серотонин;
– l‑гранулы (диаметр 200–250 нм) содержат гидролитические ферменты и рассматриваются как лизосомы.
Количество тромбоцитов в 1 мкл от 200 000 до 300 000 (200–300 109/л).
Продолжительность жизни менее 2 нед, ежедневно обновляется около 15 % от всех тромбоцитов.
Функция: остановка кровотечения при повреждении стенки сосудов путем свертывания крови (гемокоагуляция);
– участие в реакциях заживления ран и воспаления;
– обеспечение нормальной функции эндотелия сосудов (ангиотрофическая функция).
Анализ крови определяется такими понятиями, как гемограмма и лейкоцитарная формула.
Гемограмма – количественное содержание форменных элементов крови в 1 л или 1 мкл.
Гемограмма взрослого человека
Эритроциты:
у мужчин – 3,9–5,5 1012/л (3,9–5,5 106 в 1 мкл);
у женщин – 3,7–4,7 1012/л (3,7–4,7 106 в 1 мкл).
Лейкоциты – 3,8–9,0 109/л (3,8–9 103 в 1 мкл).
Тромбоциты: – 200–300 109 (200–300 103 в 1 мкл).
Лейкоцитарная формула – процентное содержание различный форм лейкоцитов (от общего числа лейкоцитов, принимаемого за 100 %).
Лейкоцитарная формула взрослого человека
Базофилы – 0,5–1 %.
Эозинофилы – 1–5 %.
Нейтрофилы – 65–75 %:
юные – 0–0,5 %;
палочкоядерные – 3–5 %;
сегментоядерные – 60–65 %.
Лимфоциты – 20–35 %.
Моноциты – 6–8 %.
Возрастные особенности крови
У новорожденных и детей гемограмма и лейкоцитарная формула отличаются от таковых у взрослых.
Гемограмма новорожденных: 1) эритроцитов 6–7 1012/л (эритроцитоз); 2) лейкоцитов 10–30 109/л (лейкоцитоз); 3) тромбоцитов 200–300 109/л, т. е. как у взрослых. Через 2 нед содержание эритроцитов приближается к показателям взрослых (около 5,0 • 1012/л). Спустя 3–6 мес число эритроцитов уменьшается (менее 4–5 • 1012/л) – физиологическая анемия, а затем постепенно достигает показателей у взрослых к периоду полового созревания.
Содержание лейкоцитов у детей через 2 нед после рождения снижается до 9–15 109/л и к периоду полового созревания достигает показателя у взрослых.
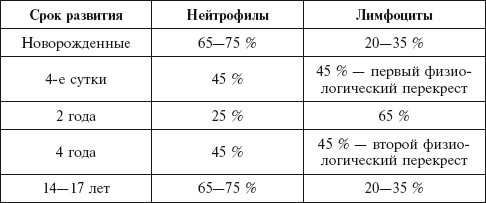
Лейкоцитарная формула новорожденных. Наибольшие изменения в лейкоцитарной формуле отмечаются в содержании нейтрофилов и лимфоцитов. Остальные показатели существенно не отличаются от показателей у взрослых (табл. 5.1).
Таблица 5.1. Лейкоцитарная формула
Кроветворение
Кроветворение (гемоцитопоэз) – процесс образования форменных элементов крови. Различают два вида кроветворения: миелоидное и лимфоидное. В свою очередь в миелоидном кроветворении выделяют: а) эритроцитопоэз; б) гранулоцитопоэз; в) тромбоцитопоэз; г) моноцитопоэз, а в лимфоидном: а) Т‑лимфоцитопоэз; б) В‑лимфоцитопоэз; в) NK‑цитопоэз.
Кроме того, гемоцитопоэз подразделяется на два периода: эмбриональный и постэмбриональный. В эмбриональном периоде гемоцитопоэза происходит образование крови как ткани, поэтому он представляет собой гистогенез крови. Постэмбриональный гемоцитопоэз – это процесс физиологической регенерации крови.
Эмбриональный период гемоцитопоэза осуществляется в эмбриогенезе поэтапно, сменяя разные органы кроветворения. Этапы перекрывают друг друга, обеспечивая тем самым непрерывность процесса. В соответствии с этим эмбриональный гемоцитопоэз подразделяется на три этапа: 1) желточный, 2) гепатотимоли‑енальный, 3) медуллярный (медуллолимфоидный).
Желточное кроветворение начинается со 2–3‑й недели эмбриогенеза: в мезенхиме желточного мешка в результате пролиферации мезенхимных клеток образуются «кровяные островки». Периферические клетки островков уплощаются (эндотелий сосуда), центральные клетки округляются и превращаются в стволовые клетки крови.
Интраваскулярно (в сосудах) образуются первичные эритробласты, первичные эритроциты (мегалобласты, мегалоциты). Экстраваскулярно из части стволовых клеток начинают развиваться в небольшом количестве зернистые лейкоциты.
В конце 3‑й недели желточная сосудистая сеть соединяется с эмбриональной (в тельце зародыша), устанавливается желточный круг кровообращения. Кровь и стволовые клетки крови поступают в сосуды зародыша, стволовые клетки заселяют закладки будущих кроветворных органов. К 12‑й неделе желточное кроветворение прекращается.
Гепатотимолиенальный этап характеризуется следующим:
– определенной органной локализацией;
– возросшими количественными и качественными параметрами крови (появляется гранулоцитопоэз, тромбоцитопоэз, моноцитопоэз и лимфоцитопоэз);
– экстраваскулярным характером;
– переходом на нормобластический тип кроветворения.
В печени с 5‑й недели до конца 5‑го месяца происходит в основном экстраваскулярное миелоидное кроветворение, которое постепенно снижается и к рождению полностью прекращается. С 7‑й недели в печени впервые появляются NK‑клетки, которые в крови обнаруживаются только с 27–28‑й недели.
Тимус очень быстро (9–12 нед) из универсального кроветворного органа становится лимфоидным, в нем начинается Т‑лимфоцитопоэз, который продолжается и после рождения до его инволюции (25–30 лет).
Селезенка с 7–8‑й недели заселяется стволовыми клетками, в ней начинается универсальное экстраваскулярное кроветворение (миело– и лимфоцитопоэз), особенно активное с 5‑го по 7‑й месяц. С 7‑го месяца миелопоэз угнетается и к рождению прекращается. Лимфоидное кроветворение локализуется вокруг артериальных сосудов органа, нарастает и продолжается в постнатальном периоде.
Медуллярный этап. Источником стволовых клеток крови со 2–3‑го месяца становится красный костный мозг. Закладка красного костного мозга появляется на 2‑м месяце эмбриогенеза, кроветворение в нем начинается с 3‑го месяца, а с 6–10‑го месяца он становится основным органом миелоидного и частично лимфоидного кроветворения, т. е. универсальным кроветворным органом. В тимусе, лимфатических узлах, селезенке в этот период осуществляется лимфоидное кроветворение. В результате последовательной смены органов кроветворения и совершенствования процесса кроветворения формируется кровь как ткань.
Постэмбриональный период гемоцитопоэза осуществляется в красном костном мозге и лимфоидных органах (тимус, лимфоидные органы, лимфатические узлы, селезенка).
Сущность процесса кроветворения заключается в пролиферации и поэтапной дифференцировке стволовых клеток в зрелые форменные элементы крови.
Общепринятой является унипотентная теория кроветворения [Максимов А. А., 1909], согласно которой все форменные элементы крови развиваются из единого предшественника – стволовой клетки.
Кроветворение в постнатальном периоде онтогенеза представлено прежде всего двумя видами кроветворения: миелоидным и лимфоидным. Каждый вид кроветворения подразделяется на разновидности или ряды кроветворения (диффероны).
Миелопоэз: а) эритроцитопоэз, или эритроцитарный ряд; б) гранулоцитопоэз, или гранулоцитарный ряд; в) моноцитопоэз, или моноцитарный ряд; г) тромбоцитопоэз, или тромбоцитарный ряд.
Лимфоцитопоэз: а) Т‑лимфоцитопоэз, или Т‑лимфоцитарный ряд; б) В‑лимфоцитопоэз, или плазмоцитопоэз.
В процессе поэтапной дифференцировки стволовых клеток в зрелые форменные элементы крови в каждом ряду кроветворения образуются промежуточные типы клеток, которые в схеме кроветворения составляют классы клеток. Всего в схеме кроветворения различают VI классов клеток: I – стволовые кроветворные клетки (СКК); II – полустволовые; III – унипотентные; IV – бластные; V – созревающие; VI – зрелые форменные элементы.
Морфологическая и функциональная характеристика клеток различных классов схемы кроветворения
Класс I – стволовая тотипотентная (плюрипотентная, полипотентная) клетка, способная к поддержанию своей популяции. По морфологии соответствует малому лимфоциту:
– обладает способностью к самоподдержанию своей популяции без притока клеток извне;
– редко делится. Деление СКК стимулируется фактором стволовых клеток, вырабатываемым стромальными клетками костного мозга;
– способна образовывать все виды форменных элементов крови;
– устойчива к действию повреждающих факторов;
– располагается в хорошо защищенных от внешних воздействий и обладающих обильным кровоснабжением местах (ячейки костной ткани);
– циркулирует в крови, мигрируя в другие органы кроветворения.
Направление дифференцировки стволовой клетки определяется содержанием в крови данного форменного элемента, а также влиянием микроокружения стволовых клеток, индуктивным влиянием стромальных (ретикулярных) клеток красного костного мозга или другого кроветворного органа, вырабатывающего гемопоэтические факторы роста (гемопоэтины).
Поддержание численности популяции стволовых клеток обеспечивается тем, что после митоза стволовой клетки одна из дочерних клеток становится на путь дифференцировки, а другая принимает морфологию малого лимфоцита и остается стволовой.
Делятся стволовые клетки редко (их интерфаза составляет 1–2 года): 80 % стволовых клеток находятся в состоянии покоя и только 20 % – в митозе и последующей дифференцировке.
В процессе пролиферации в культуре костного мозга или селезенке каждая стволовая клетка образует группу, или клон, клеток, поэтому стволовые клетки в литературе нередко называют колониеобразующими единицами – КОЕ‑С.
Класс II – полустволовые, ограниченно полипотентные или мультипотентные (частично коммитированные) клетки – предшественницы: а) миелопоэза – КОЕ‑ГЭММ; б) лимфоцитопоэза – КОЕ‑Л, или Лск; в) NK‑цитопоэза. Имеют морфологию малого лимфоцита. Каждая из них дает клон клеток, но только миелоидных или лимфоидных. Делятся чаще (через 3–4 нед) и также поддерживают численность своей популяции.
Класс III – олигопотентные (КОЕ‑ГМ) и унипотентные (прогениторные) поэтинчувствительные клетки – предшественницы своего ряда кроветворения: КОЕ‑М, КОЕ‑Гн, КОЕ‑Эо, КОЕ‑Б, КОЕ‑Мег и КОЕ‑Э. Морфология их также соответствует морфологии малого лимфоцита. Способны дифференцироваться только в один тип форменного элемента.
Делятся часто, но одни потомки этих клеток вступают на путь дифференцировки, а другие сохраняют численность популяции клеток данного класса.
Частота деления этих клеток и способность дифференцироваться дальше зависят от содержания в крови особых биологически активных веществ – поэтинов, специфичных для каждого ряда кроветворения (эритропоэтины, тромбоцитопоэтины и др.).
Первые три класса клеток объединяются в класс морфологически неидентифицируемых клеток, так как все они имеют морфологию малого лимфоцита, но потенции их к развитию различны.
Класс IV – бластные (молодые) клетки, или бласты (эритробласты, лимфобласты и т. д.). Отличаются по морфологии как от трех предшествующих, так и от последующих классов клеток.
Эти клетки крупные, имеют большое рыхлое богатое эухроматином ядро с 2–4 ядрышками, цитоплазма базофильная за счет большого числа свободных рибосом. Часто делятся, но дочерние клетки все вступают на путь дальнейшей дифференцировки. По цитохимическим свойствам можно идентифицировать бласты разных рядов кроветворения.
Класс V – класс созревающих (дифференцирующихся) клеток, характерных для своего ряда кроветворения. В этом классе может быть несколько разновидностей переходных клеток – от одной (пролимфоцит, промоноцит) до пяти – в эритроцитарном ряду. Некоторые созревающие клетки в небольшом количестве (см. лейкоцитарную формулу гранулоцитов) могут попадать в кровь (например, ретикулоциты, юные и палочкоядерные гранулоциты).
Класс VI – зрелые форменные элементы крови. Следует отметить, что только эритроциты, тромбоциты и сегментоядерные гранулоциты являются зрелыми конечными дифференцированными форменными элементами или их фрагментами.
Моноциты – не окончательно дифференцированные клетки. Покидая кровеносное русло, они дифференцируются в тканях в конечные клетки – макрофаги. Лимфоциты при встрече с антигенами превращаются в бласты и снова делятся.
Совокупность клеток, составляющих линию дифференцировки стволовой клетки в определенный форменный элемент, образует его дифферон, или гистогенетический ряд. Например, эритроцитарный дифферон (эритрон) составляют: I класс – стволовая клетка (СК); II класс – полустволовая клетка (ПСК) – предшественница миелопоэза; III класс – унипотентная эритропоэтин‑чувствительная клетка – КОЕ‑Э, сюда же относят бурстобразующую единицу – БОЕ‑Э, способную быстро (взрывоподобно) образовывать колонию эритроидных клеток численностью в несколько сотен элементов; IV класс – проэритробласт; V класс – созревающие клетки: базофильный, полихроматофильный, оксифильный нормоцит; VI класс – эритроцит.
В процессе созревания эритроцитов в V классе происходят: а) синтез и накопление гемоглобина, б) редукция органелл, в) редукция ядра.
В норме пополнение эритроцитов происходит в основном за счет деления и дифференцировки созревающих клеток – пронормоцитов, базофильных и полихроматофильных нормоцитов. Такой тип кроветворения носит название гомопластического кроветворения. Клеточные элементы, составляющие диффероны других форменных элементов крови, каждый студент должен уметь перечислить по схеме кроветворения.
Гранулоцитопоэз
Гранулоциты существуют трех типов, каждый из которых происходит от собственной унипотентной стволовой клетки, производной КОЕ‑ГЭММ (колониеобразующей единицы гранулоцитов, эритроцитов, моноцитов и мегакариоцитов), образующей гистологически определенный миелобласт.
Образование нейтрофилов: I класс (СК) II класс (ПСК)
III класс (унипотентная лейкопоэтинчувствительная клетка – КОЕ‑Гн) IV класс (нейтрофильный миелобласт) V класс (нейтрофильный промиелоцит, нейтрофильный миелоцит, нейтрофильный метамиелоцит, палочкоядерный нейтрофил)
VI класс (зрелый нейтрофил).
Нейтрофильный миелобласт (IV класс) диаметром от 12 до 14 мкм, его крупное округлое красновато‑синее ядро имеет тонкую сеть хроматина, присутствуют два или три бледно‑серых ядрышка, цитоплазма не имеет гранул;
– на периферии клетки часто имеются цитоплазматические выпячивания, похожие на псевдоподии (определяются на электронных микрофотографиях);
– в цитоплазме присутствуют гранулярная эндоплазматическая сеть, небольшой комплекс Гольджи, множество митохондрий и свободных рибосом.
Нейтрофильный промиелоцит (V класс) крупнее миелобласта (диаметр 16–24 мкм). Ядро имеет грубую сеть хроматина и 1–2 ядрышка;
– цитоплазма голубоватого оттенка, содержит множество азурофильных гранул (неспецифических), периферия клетки больше не имеет похожих на псевдоподии цитоплазматических выпячиваний. На электронных микрофотографиях видны хорошо развитый комплекс Гольджи, гранулярная эндоплазматическая сеть и множество митохондрий;
– азурофильные гранулы диаметром примерно 0,5 мкм, формируются на поверхности созревающего комплекса Гольджи. Это лизосомы, содержащие гидролитические ферменты и пероксидазу.
Нейтрофильный миелоцит диаметром 10–12 мкм; имеет немного уплощенное ацентричное ядро с грубой сетью хроматина. Ядрышки могут быть, а могут отсутствовать;
– специфические гранулы диаметром 0,1 мкм, содержат лизоцим, щелочную фосфатазу, коллагеназу и фагоцитин, ясно видны, как и азурофильные гранулы;
– комплекс Гольджи хорошо развит, выглядит как прозрачный чистый участок в бледно‑голубой цитоплазме;
– на поверхности формирования комплекса Гольджи образуются специфические нейтрофильные гранулы;
– все еще происходит клеточное деление. Это единственная стадия, на которой формируются специфические нейтрофильные гранулы.
Нейтрофильный метамиелоцит похож на нейтрофильный миелоцит, за исключением того, что ядро бобовидное и грубая сеть хроматина не имеет ядрышек (рис. 5.3);
– гетерохроматин указывает на уменьшение синтеза белка, что отражается в редукции органелл в клетке.
Палочкоядерный нейтрофил похож на зрелый нейтрофил, за исключением подковообразного ядра. Палочкоядерные клетки часто находят в циркулирующей крови, а в случаях инфицирования организма их число резко увеличивается.
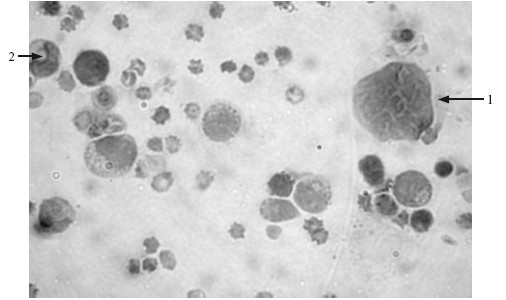
Рис. 5.3. Мазок красного костного мозга. ×1200.
1 – мегакариобласт; 2 – метамиелоцит.
Количество нейтрофилов, продуцируемый: в организме здорового взрослого человека, около 800 000 в день.
Образование эозинофилов и базофилов: стадии развития эозинофилов и базофилов похожи на стадии, описанные для нейтрофилов, за исключением того, что типы гранул, формирующихся на стадии миелоцита, специфичны для каждого типа клеток. Кроме того, морфология ядра зрелой клетки напоминает таковую на поздней стадии палочкоядерного гранулоцита.
Моноцитопоэз: I класс (СК) → II класс (ПСК) → III класс (унипотентная клетка – КОЕ‑М) – общая предшественница моноцитов и нейтрофилов (дает начало монобластам) → IV класс (монобласты) → V класс (промоноцит) → VI класс (моноцит).
Промоноцит – крупная клетка (диаметр 16–18 мкм) с несколько бобовидным ядром, расположенным эксцентрично в светло‑голубой цитоплазме, которая содержит также множество азурофильных гранул (лизосом), продуцируемых хорошо развитым комплексом Гольджи, многочисленные митохондрии и довольно развитую гранулярную эндоплазматическую сеть.
Деление промоноцитов приводит к формированию моноцитов (VI класс), которые покидают костный мозг, поступают в кровоток, а затем после проникновения в соединительную ткань периферических органов дифференцируются в макрофаги, а также в дендритные антигенпредставляющие клетки.
Количество моноцитов, образующихся ежедневно в организме здорового взрослого человека, составляет около 1 1010.
Образование кровяных пластинок (тромбоцитопоэз): I класс (СК) → II класс (ПСК) → III класс (унипотентная тромбопоэтинчувствительная клетка – КОЕ‑мег) → IV класс (мегакариобласт) → V класс (промегакариоцит) → VI класс (тромбоцитах).
Мегакариобласт – крупная клетка (диаметр 25–40 мкм), единственное крупное ядро с выемками (либо дольчатое) имеет тонкую сеть хроматина. Деление мегакариобласта происходит путем эндомитоза, в его ходе не образуется дочерних клеток. Вместо этого клетка приобретает гигантские размеры, плоидность ядра может достигать 64 (см. рис. 5.2);
– цитоплазма слабобазофильная, без гранул, на электронных микрофотографиях видны крупные митохондрии, многочисленные полисомы, некоторое количество гранулярной эндоплазматической сети и довольно хорошо развитый комплекс Гольджи.
Промегакариоцит – крупная округлая клетка диаметром 42–45 мкм с объемным дольчатым полиплоидным ядром и резко базофильной цитоплазмой;
– помимо обычных органелл, цитоплазма содержит сложную систему гладких пузырьков, тубул, плоских цистерн, которые, сливаясь, формируют тромбоцитарные демаркационные каналы;
– в процессе дальнейшей дифференцировки промегакариоциты становятся либо резервными, либо тромбоцитпродуцирующими мегакариоцитами.
Мегакариоцит – необычайно крупная клетка (диаметр 40– 100 мкм) с одним многодольчатым крупным полиплоидным ядром. На электронных микрофотографиях видны хорошо развитый комплекс Гольджи, активно формирующий α‑гранулы, лизосомы и плотные тельца, многочисленные митохондрии и довольно развитая гранулярная эндоплазматическая сеть.
Мегакариоциты расположены в окружности синусоидов, в поры стенки которых проникают их отростки. Отростки распадаются вдоль определенных демаркационных каналов, формируя группы соединенных кровяных пластинок, которые затем разделяются на отдельные тромбоциты.
После полного отделения тромбоцитов остаточные мегакариоциты подвергаются дегенерации, фагоцитируются и замещаются новыми.
Лимфоцитопоэз
Клетка‑предшественница лимфоцитов берет начало от популяции СК (тотипотентные гемопоэтические стволовые клетки), находится в костном мозге, как и в циркулирующей крови, как член популяции «нулевых» клеток.
Это иммунокомпетентные клетки, дающие начало по меньшей мере двум популяциям СК: клеткам‑предшественницам Т‑лимфоцитов и клеткам‑предшественницам В‑лимфоцитов и, наверное, клеткам‑предшественницам NK‑клеток (естественные киллеры).
В Т– и В‑лимфоцитопоэзе выделяют три этапа: I – костно‑мозговой этап; II – антигеннезависимой дифференцировки (в центральных иммунных органах); III – антигензависимой дифференцировки (в периферических органах иммунной защиты).
Т‑лимфоцитопоэз. Этап I протекает в лимфоидной ткани красного костного мозга: I класс (СК) II класс (ПСК) – клетки‑предшественницы лимфопоэза – КОЕ‑Л, или Лск, III класс (унипотентные Т‑поэтинчувствительные клетки – клетки‑предшественницы Т‑лимфоцитопоэза). Эти клетки с током крови достигают тимуса./
Этап II осуществляется в корковом веществе тимуса под влиянием тимозина: унипотентные клетки‑предшественницы (III класс) превращаются в Т‑лимфобласты (IV класс), затем в Т‑пролимфоциты (V класс) и в Т‑лимфоциты (VI класс). В тимусе развиваются самостоятельно три субпопуляции Т‑лимфоцитов: киллеры, хелперы, супрессоры, приобретающие разные рецепторы к разнообразным антигенам. Они током крови заносятся в периферические лимфоидные органы.
Этап III протекает в Т‑зонах периферических лимфоидных органов. Под влиянием соответствующего антигена Т‑лимфоцит превращается в Т‑лимфобласт, вернее Т‑иммунобласт (реакция бласттрансформации). Затем эти клетки пролиферируют и образуют клоны клеток: Т‑клетки памяти, Т‑киллеры, Т‑хелперы и т. д., т. е. эффекторные клетки, обеспечивающие клеточный иммунитет. При повторной встрече с антигеном Т‑лимфоциты памяти всех субпопуляций обеспечивают более быстрый и сильный вторичный иммунный ответ.
В‑лимфоцитопоэз и плазмоцитопоэз. Этап I осуществляется в красном костном мозге, где образуются следующие классы клеток: I (СК) → II (ПСК) – предшественницы лимфопоэза → III класс – унипотентные В‑лимфопоэтинчувствительные клетки – предшественницы В‑лимфоцитопоэза.
Этап II – антигеннезависимой дифференцировки – у птиц осуществляется в специальном центральном лимфоидном органе – фабрициевой сумке. Его аналог у человека точно не установлен. Большинство исследователей считают, что II этап также происходит в красном костном мозге: из унипотентных В‑клеток‑предшественниц образуются В‑лимфобласты (IV класс), В‑пролимфоциты (V класс) и В‑лимфоциты рецепторные (VI класс). В‑лимфоциты приобретают на этом этапе разнообразные рецепторы к антигенам – иммуноглобулины, которые синтезируются в самих созревающих В‑лимфоцитах.
Этап III – антигензависимой дифференцировки – происходит в В‑зонах периферических лимфоидных органов, где происходят встреча антигена с соответствующим В‑рецепторным лимфоцитом, активация и трансформация последнего в иммунобласт – плазмобласт, а затем образуется клон клеток, среди которых различают:
– В‑лимфоциты памяти;
– плазмоциты, которые являются эффекторными клетками гуморального иммунитета. Они синтезируют и выделяют в кровь или лимфу иммуноглобулины (антитела) разных классов, которые образуют комплексы антиген – антитело, нейтрализуя антигены. Иммунные комплексы затем фагоцитируются нейтрофилами и макрофагами.
Для реакции бласттрансформации В‑лимфоцита необходима кооперация В‑рецепторного лимфоцита, макрофага, Т‑хелпера (Т‑супрессора), а также гуморального антигена.
Развитие NK‑клеток происходит независимо от образования Т– и В‑лимфоцитов из костно‑мозгового предшественника;
– после выхода в кровь NK‑клетки циркулируют в ней или мигрируют в селезенку;
– дозревание NK‑клеток происходит в тканях под влиянием малоизученных факторов микроокружения.
Тесты и вопросы для самоконтроля
1. Сущность кроветворения.
2. Периоды кроветворения.
3. Виды (ветви) кроветворения.
4. Разновидности миелоидного кроветворения.
5. Разновидности лимфоидного кроветворения.
6. Этапы и органы эмбрионального кроветворения.
7. Сущность эмбрионального кроветворения.
8. Сущность постэмбрионального кроветворения.
9. Перечислить классы клеток в процессе кроветворения.
10. Ряды (диффероны) кроветворения в схеме кроветворения.
11. Эритроцитарный дифферон.
12. Тромбоцитарный дифферон.
13. Гранулоцитарный дифферон.
14. Моноцитарный дифферон.
15. Т‑лимфоцитарный дифферон.
16. В‑лимфоцитарный дифферон.
17. Отличие лимфоидного кроветворения от миелоидного.
18. Этапы и локализация лимфопоэза.
19. Т‑лимфоцитопоэз (этапы, локализация, клетки).
20. Сущность этапа антигеннезависимой дифференцировки Т– и В‑лимфоцитов.
21. Процессы и сущность этапа антигензависимой дифференцировки Т‑лимфоцитов.
22. В‑лимфоцитопоэз (этапы, локализация).
23. Процессы и сущность этапа антигензависимой дифференцировки В‑лимфоцитов.
24. Определение понятия «гуморальный иммунитет».
25. Эффекторные клетки гуморального иммунитета.
26. Определение понятия «клеточный иммунитет».
27. Эффекторные клетки клеточного иммунитета.
28. Кооперация клеток в гуморальном иммунитете.
Ответы
1. Процесс пролиферации и поэтапной дифференцировки стволовых клеток в зрелые форменные элементы крови.
2. Эмбриональный; постэмбриональный.
3. Миелоидное; лимфоидное.
4. Эритроцитопоэз; гранулоцитопоэз; тромбоцитопоэз; моноцитопоэз; развитие предшественников Т– и В‑лимфоцитопоэза.
5. Т‑лимфоцитопоэз; В‑лимфоцитопоэз и плазмоцитопоэз.
6. Желточный (мегалобластический); гепатотимолиенальный; медуллярный.
7. Разновидность гистогенеза – образование крови как ткани.
8. Процесс физиологической регенерации крови.
9. I класс – стволовая полипотентная клетка; II класс – полустволовая клетка‑предшественница: миело– и лимфоцитопоэза; III класс – унипотентная поэтинчувствительная клетка‑предшественница своего кроветворения; IV класс – бласты; V класс – созревающие клетки; VI класс – зрелые форменные элементы крови.
10. Эритроцитарный ряд – эритроцитопоэз; гранулоцитарный ряд; моноцитарный ряд; тромбоцитарный ряд; Т‑лимфоцитопоэз; В‑лимфоцитопоэз.
11. Стволовая клетка; полустволовая клетка‑предшественница миелопоэза; унипотентная поэтинчувствительная клетка; эритробласт; класс созревающих клеток: пронормоцит, базофильный нормоцит, полихроматофильный нормоцит, оксифильный нормоцит; ретикулоцит, эритроцит.
12. Стволовая клетка; полустволовая клетка‑предшественница миелопоэза; унипотентная тромбопоэтинчувствительная клетка; мегакариобласт; промегакариоцит; мегакариоцит; тромбоцит.
13. Стволовая клетка; полустволовая клетка‑предшественница миелопоэза; унипотентная гранулоцитопоэтинчувствительная клетка; миелобласт; промиелоцит; миелоцит; метамиелоцит (юный); палочкоядерный; сегментоядерный нейтрофил, эозинофил, базофил.
14. Стволовая клетка; полустволовая клетка‑предшественница миелопоэза; унипотентная; монобласт; промоноцит; моноцит; макрофаг.
15. Стволовая клетка; полустволовая клетка‑предшественница лимфопоэза; унипотентная Т‑лимфопоэтинчувствительная клетка; Т‑лимфобласт; Т‑пролимфоцит; Т‑лимфоцит.
16. Стволовая клетка; полустволовая клетка‑предшественница лимфопоэза; унипотентная В‑лимфопоэтинчувствительная клетка; В‑лимфобласт; В‑пролимфоцит; В‑лимфоцит.
17. Развивается поэтапно, сменяя разные органы.
18. I этап – в красном костном мозге; II этап – антигеннезависимой дифференцировки в центральных иммунных органах: тимусе, фабрициевой сумке или ее аналоге; III этап – антигензависимой дифференцировки в периферических лимфоидных органах (лимфатические узлы, селезенка).
19. I этап – в красном костном мозге. Клетки: 1) стволовая, 2) полустволовая клетка‑предшественница лимфопоэза, 3) унипотентная Т‑лимфопоэтинчувствительная; II этап – антигеннезависимой дифференцировки осуществляется в тимусе. Клетки: а) Т‑лимфобласт, б) Т‑пролимфоцит, в) Т‑лимфоцит (киллер, хелпер, супрессор); III этап – антигензависимой дифференцировки в Т‑зонах лимфатических узлов и селезенки. Клетки: Т‑лимфоциты (киллер, хелпер, супрессор) + макрофаг + антиген → реакция бласттрансформации и пролиферации и образования: 1) Т‑клеток памяти, 2) Т‑киллеров, 3) Т‑хелперов, 4) Т‑супрессоров.
20. Образование рецепторных (Т– и В‑лимфоцитов), осуществляющих иммунологический надзор в организме – распознавание «своих» и «чужих» клеток.
21. Встреча Т‑лимфоцита (киллера, хелпера, супрессора) с антигеном с помощью макрофага; бласттрансформация; пролиферация; образование эффекторных Т‑лимфоцитов: Т‑клеток памяти, Т‑киллеров, Т‑хелперов и Т‑супрессоров.
22. I этап – в красном костном мозге. Клетки: а) стволовая, б) полустволовая клетка‑предшественница лимфопоэза, в) унипотентная В‑лимфопоэтинчувствительная; II этап – антигеннезависимой дифференцировки – осуществляется в фабрициевой сумке или ее аналоге (красный костный мозг). Клетки: а) В‑лимфобласт, б) В‑пролимфоцит, в) В‑лимфоцит; III этап – антигензависимой дифференцировки в В‑зонах лимфатических узлов и селезенке. Клетки: В‑лимфоциты + макрофаг + антиген + Т‑хелпер – реакция бласттрансформации и пролиферации и образование В‑клеток памяти и плазмоцитов.
23. Встреча В‑лимфоцита с антигеном с помощью макрофага и Т‑хелпера; бласттрансформация; пролиферация; образование плазмоцитов и В‑клеток памяти.
24. Защита организма от корпускулярных генетически чужеродных веществ (бактерии, вирусы, белки, полисахариды).
25. В‑лимфоциты; плазмоциты.
26. Защита организма от чужеродных клеток, трансплантированных или собственных (генетически измененных).
27. Т‑киллеры.
28. В‑лимфоциты; макрофаг; Т‑хелперы или Т‑супрессоры.
Глава 6
Хрящевые и костные ткани
Хрящевые и костные ткани – специализированные типы соединительной ткани, объединенные в группу скелетных тканей на основании ряда признаков: общей (опорной) функции, общего источника развития в эмбриогенезе (мезенхимы) и сходства строения – образованы клетками и преобладающим по объему межклеточным веществом. Каждая из них имеет характерные основное вещество, набор волокон и клетки:
– основное вещество хрящевой ткани твердое, но упругое;
– основное вещество костной ткани кальцинировано и у высших позвоночных образует скелет.
И кость, и хрящ выполняют опорную функцию, но кость также служит депо кальция и фосфатов, защищает жизненно важные органы и содержит костный мозг.
Хрящевые ткани
Хрящевая ткань (textus cartilagineus) составляет около 2 % от массы тела; входит в состав дыхательной системы (нос, гортань, трахея, бронхи), ушной раковины, ребер, суставов, межпозвоночных дисков и т. д.
Состоит из клеток (хондроциты) и межклеточного вещества (матрикс), образованного коллагеновыми волокнами (в эластическом хряще также и эластическими) и основным аморфным веществом.
В состав аморфного вещества входят протеогликаны, образующие крупные агрегаты, и гликопротеины.
В хрящевых тканях отсутствуют сосуды.
Хрящевые ткани характеризуются некоторыми общими структурно‑функциональными свойствами:
– высоким (до 75–85 %) содержанием воды в матриксе;
– сравнительно низким уровнем метаболизма;
– способностью к непрерывному росту;
– прочностью и эластичностью (способность к обратимой деформации).
Хрящевые ткани образуют структуры органного порядка – хрящи. Выделяют три вида хрящей: гиалиновый, эластический и волокнистый.
Гиалиновый хрящ (cartilago hyalina) локализуется в ребрах, суставах, стенке воздухоносных путей. У плода формирует скелет, в растущем организме и при переломах кости – место образования костной ткани. Состоит из хрящевых клеток и хрящевого матрикса (рис. 6.1).
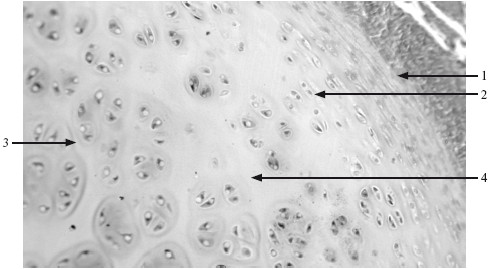
Рис. 6.1. Гиалиновый хрящ. ×270.
1 – надхрящница; 2 – молодые хондроциты; 3 – изогенные группы хрящевых клеток в зоне зрелого хряща; 4 – межклеточное вещество.
Матрикс состоит из аморфного вещества, коллагеновых волокон и интерстициальной воды. Содержит до 75 % воды, что позволяет веществам из сосудов надхрящницы диффундировать к клеткам. Сам хрящ не содержит сосудов.
♥ Белки хрящевого матрикса
Коллагены:
тип II образует коллагеновые волокна, составляет до 40 % от сухой массы хряща;
– направление волокон в пространстве обычно соответствует направлению сил, воздействующих на хрящ;
– коллагеновый каркас хрящевого матрикса обладает большой упругостью и высокой прочностью;
тип IX сшивает коллагеновые волокна, его в 5 раз меньше, чем коллагена II типа;
– имеется небольшое количество коллагена типов VI и X;
– секретируются хондроцитами;
– у взрослого коллагеновые волокна в гиалиновом хряще не обновляются, что может способствовать старению.
Протеогликаны – гигантские молекулы, секретируемые хондроцитами, состоят из белков (10–20 %) и на 80–90 % из гликозаминогликанов;
– главная функция – связывание воды и обеспечение диффузии веществ;
– состоят из гиалуроновой кислоты, связанной с белком, и множества полисахаридных цепей. В их состав входят также сульфатированные гликозаминогликаны: хондроитинсульфаты, гепарансульфаты и др.;
– связывают отдельные компоненты матрикса в единую систему, усиливая взаимодействие между адгезивными белками хрящевого матрикса (анкорин, хондронектин) и коллагеном;
– хондронектин имеет участки связывания коллагена II типа, протеогликанов и рецепторов хондронектина в плазмолемме хондроцитов, т. е. связывает хондроциты и коллаген II типа.
Типы хрящевого матрикса:
– территориальный (капсулярный) окружает изогенные группы хрящевых клеток, базофилен и метахроматичен, беден коллагеном, но богат гликозаминогликанами;
– коллагеновые волокна ориентированы на поверхности клеточных групп, образуя стенку лакун;
– внутри лакун пространства между клетками заполнены протеогликанами;
– интертерриториальный расположен между изогенными группами, содержит меньше гликозаминогликанов, но больше коллагена;
– характеризуется слабобазофильной или оксифильной окраской;
– коллагеновые волокна ориентированы вдоль направления действия механических сил на хрящ;
– интерстициальная вода обладает способностью перемещаться в пределах матрикса хряща;
– содержит растворенные в ней ионы и низкомолекулярные белки;
– благодаря своей несжимаемости обеспечивает жесткость хрящевой ткани.
Надхрящница – соединительная ткань, окружающая хрящ, кроме суставных поверхностей.
Состоит из наружного толстого волокнистого слоя, содержащего коллаген I типа, фибробласты и кровеносные сосуды, и тонкого внутреннего клеточного (хондрогенного) слоя.
Наружный слой образован плотной волокнистой неоформленной соединительной тканью; обеспечивает механическую прочность надхрящницы, ее связь с другими структурами.
Внутренний слой состоит из рыхлой волокнистой соединительной ткани с высоким содержанием клеток; в нем располагается сосудистая сеть, питающая хрящ, и камбиальные (хондрогенные) клетки.
Хондрогенные клетки во внутреннем слое надхрящницы дифференцируются в хондробласты, которые продуцируют хрящ.
Хондроциты – зрелые хрящевые клетки, расположенные в лакунах хряща и окруженные матриксом;
– оси поверхностно расположенных хондроцитов параллельны поверхности хряща, это клетки овальной формы;
– хондроциты, лежащие глубже, более старые, имеют сферическую форму и располагаются в виде изогенных групп (от 4 до 8 клеток).
На электронной микрофотограмме хондроциты имеют неровную поверхность с небольшими выступами, хорошо развитые гранулярную эндоплазматическую сеть и комплекс Гольджи. Многочисленные вакуоли содержат коллагены и протеогликаны.
Гистофизиология:
– хондроциты производят основное вещество и коллаген;
– на рост хряща влияют гормоны: тироксин, тестостерон, СТГ, увеличивающие скорость роста, и кортизол, гидрокортизон, эстрадиол, уменьшающие скорость роста.
Гистогенез: в организме эмбриона мезенхимные клетки дифференцируются в хондробласты. Эти базофильные клетки секретируют матрикс и заключаются в него, становясь хондроцитами;
интерстициальный рост (рост изнутри) происходит только в молодом хряще при делении клеток внутри хряща (образование изогенных групп);
аппозиционный рост происходит при дифференцировке хондрогенных клеток надхрящницы в хондробласты, формирующие новый слой хряща по периферии уже существующего.
Регрессивные изменения гиалиновый хрящ претерпевает с возрастом. Клетки гипертрофируются и гибнут, а основное вещество кальцифицируется.
Гиалиновый хрящ регенерирует с трудом, часто надхрящница формирует рубцовую ткань.
Эластический хрящ (cartilago elastica) входит в состав ушной раковины, слуховой (евстахиевой) трубы, надгортанника, рожковидных и клиновидных хрящей гортани (рис. 6.2). Помимо прочности и упругости обладает эластичностью, т. е. способностью к обратимой деформации;
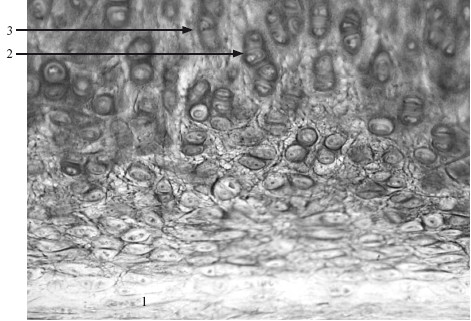
Рис. 6.2. Эластический хрящ. ×130.
1 – надхрящница; 2 – изогенные группы хрящевых клеток; 3 – эластические волокна.
– принципиально построен так же, как гиалиновый. Главное отличие – присутствие в хрящевом матриксе сети эластических волокон вариабельной толщины (0,2–5,0 мкм), вследствие чего он имеет желтоватый оттенок;
– хондроциты располагаются в лакунах поодиночке или в виде небольших (2–4) изогенных групп;
– хондроциты вырабатывают, помимо коллагена II типа и сульфатированных гликозаминогликанов, белок эластин и специфические гликопротеины;
– эластин образует более 90 % белков межклеточного вещества;
– по сравнению с гиалиновым, эластический хрящ менее подвержен дегенерации, содержит меньше липидов, гликогена, хондроитинсульфатов и не обызвествляется.
Волокнистый хрящ (cartilago fibrosa) присутствует в межпозвоночных и суставных дисках, лобковом симфизе, а также в участках прикрепления некоторых сухожилий и связок к костям или гиалиновым хрящам (рис. 6.3). Надхрящницы не имеет;

Рис. 6.3. Волокнистый хрящ. ×400.
1 – хондроциты; 2 – коллагеновые волокна; 3 – гиалиновый хрящ.
– структурно занимает промежуточное положение между сухожилием и гиалиновым хрящом, часто граничит с ними или входит в состав тех и других;
– коллагеновые волокна расположены параллельно друг другу в соответствии с вектором действия механических сил. Между ними лежат цепочки хрящевых клеток;
– хондроциты округлые или удлиненной формы, располагаются в лакунах поодиночке или в виде мелких изогенных групп, которые выстраиваются в колонки вдоль пучков коллагеновых волокон;
– продуцируют, помимо коллагена II типа и компонентов основного вещества хряща, значительное количество коллагена I типа;
– хрящ испытывает значительные механические нагрузки как при сжатии, так и при растяжении;
– хрящ никогда не выявляется изолированно, он всегда переходит в плотную волокнистую соединительную ткань или гиалиновую хрящевую ткань.
Костные ткани
Костная ткань (textus osseus) формирует кости скелета организма, защищает и поддерживает жизненно важные органы, выполняет функцию депо кальция, содержит до 99 % его запасов в организме;
– образована клетками и обызвествленным межклеточным веществом (матрикс).
Матрикс составляет 50 % от сухой массы кости и состоит из неорганической (50 %), органической (25 %) частей и воды (25 %);
– неорганическая часть в значительной мере состоит из фосфора и кальция, образующего кристаллы гидроксиапатита Са10(РО4)6(ОН)2, имеющие стандартный размер 30 × 5 × 1,5 нм и соединяющиеся с молекулами коллагена через оссеонектин. В состав неорганической части входят также бикарбонаты, нитраты, фториды, соли магния, калия, кальция и т. д.;
– органическая часть образована коллагеном I (90–95 %) и V типов, а также неколлагеновыми белками (оссеонектин, остеокальцин, костный сиалопротеин, оссеопонтин, а также цитокины, факторы роста, протеогликаны, фосфопротеины и др.) и гликозаминогликанами (хондроитин‑4‑сульфат, хондроитин‑6‑сульфат, кератансульфат);
– органические вещества костного матрикса синтезируются фибробластами.
♦ Клетки костной ткани
Остеогенные клетки‑предшественницы происходят из мезенхимы, веретеновидные, расположены в периосте и эндосте;
– при высоком давлении кислорода дифференцируются в остеобласты, при низком – в хондрогенные клетки.
Остеобласты развиваются из остеогенных клеток; различают активную и неактивную формы остеобластов;
– активные остеобласты имеют кубическую форму, базофильную цитоплазму;
– синтезируют и секретируют вещества костного матрикса (остеоид), в связи с чем имеет хорошо развитую гранулярную эндоплазматическую сеть и комплекс Гольджи;
– в состав остеоида входят коллаген I типа (90 % от всех образуемых ими белков), в небольшом количестве коллагены III, IV, V, XI, XIII типов (5 % белков), ряд неколлагеновых белков (гликопротеины: остеонектин, остеопонтин, протеогликаны: бигликан, декорин, гиалуроновая кислота);
– активные остеобласты продуцируют также цитокины, различные факторы роста, ферменты (щелочная фосфатаза, коллагеназа), фосфопротеины;
– с помощью коротких отростков, содержащих актиновые микрофиламенты, активные клетки устанавливают контакты с соседними остеобластами и остеоцитами;
– в остеобластах высока активность щелочной фосфатазы, необходимой для минерализации матрикса;
– остеобласты выделяют матриксные пузырьки, содержащие липиды, Са2+, щелочную фосфатазу, коллагеназу, с помощью которых происходит оссификация остеоида;
– неактивные (покоящиеся) остеобласты в покоящейся кости покрывают 80–95 % ее поверхности;
– образуются из активных остеобластов путем редукции органелл и уплощения ядер и формы;
– вместе с остеоцитами образуют систему, регулирующую минеральный обмен костной ткани;
– играют важную роль в инициации перестройки костной ткани.
Остеоциты – зрелые неделящиеся клетки. Это основной тип клеток зрелой костной ткани; расположены в костных лакунах;
– имеют тонкие отростки, расположенные в канальцах, отходящих в разные стороны от лакун и контактирующие с отростками других остеоцитов с помощью щелевых соединений (передача низкомолекулярных питательных веществ и ионов);
– совокупность канальцев и лакун – лакунарно‑канальцевая система дополнена тканевой жидкостью, через которую осуществляется обмен между остеоцитами и кровью.
Функция: остеоциты поддерживают структурную целостность минерализованного матрикса, участвуют в регуляции обмена кальция и фосфора в организме.
Остеокласты – крупные клетки (20–100 мкм), происходят из моноцитов путем их слияния и образования больших многоядерных (содержащих до 50 ядер) клеток, способных перемещаться в костном матриксе;
– располагаются в образованных ими углублениях на поверхности костной ткани (резорбционных лакунах, или лакунах Гаушипа) поодиночке или небольшими группами;
– остеокласты – резко поляризованные клетки. В активном остеокласте различают 4 зоны:
– гофрированная каемка – многочисленные цитоплазматические выросты, направленные к поверхности кости, через которые выделяется большое количество Н+, что создает в лакуне кислую среду, оптимальную для растворения солей кальция и костного матрикса;
– образование Н+ в цитоплазме катализирует карбоангидраза;
– выделяются также кислые гидролазы, коллагеназы и другие протеолитические ферменты, расщепляющие органическую часть костного матрикса;
– светлая зона остеокласта с помощью актиновых филаментов плотно прилегает к костной ткани, создавая замкнутое пространство в лакуне, необходимое для создания высокой концентрации Н+ и ферментов;
– везикулярная зона содержит многочисленные лизосомы;
– базальная зона содержит ядро и органеллы;
– регуляция активности остеокластов обеспечивается гормоном околощитовидных желез (паратгормон), активирующим остеокласты, и гормоном щитовидной железы (кальцитонин), который угнетает их деятельность;
– на образование и активность остеокластов влияют также женские половые гормоны (эстрогены), простагландины, ряд интерлейкинов и факторов роста.
Классификация
Различают: грубоволокнистую (первичную, незрелую) и пластинчатую (зрелую) костные ткани;
– микроскопически в кости выделяют губчатое и компактное вещество. Губчатая кость состоит из губчатого вещества и тонкого слоя компактного вещества. Губчатое вещество формирует внутреннюю часть кости. Это масса костных трабекул, окружающая полости, заполненные костным мозгом. Трабекула содержит остеоциты и окружена снаружи одним слоем остеобластов;
– компактное вещество (кортикальная кость) сравнительно плотное, тяжелое, составляет 80 % от массы скелета взрослого человека;
– состоит из костных пластинок, образующих: остеоны; вставочные (интерстициальные) пластинки; наружные и внутренние общие (генеральные) пластинки.
Грубоволокнистая костная ткань:
– между толстыми пучками коллагеновых волокон, идущих в различных направлениях, расположены остеоциты;
– характерно наличие в костном матриксе большого количества протеогликанов и гликопротеинов, низкое содержание минеральных солей;
– присутствует в основном у плода в ходе нормального развития, постепенно замещаясь пластинчатой костной тканью;
– у взрослых сохраняется в местах прикрепления сухожилий к костям, в заросших черепных швах, зубных альвеолах, костном лабиринте внутреннего уха.
Пластинчатая костная ткань (рис. 6.4):
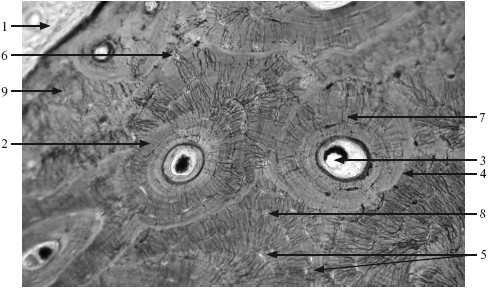
Рис. 6.4. Пластинчатая кость; поперечный разрез. ×100.
1 – надкостница; 2 – остеон; 3 – гаверсов канал; 4 – спайная линия; 5 – костные полости; 6 – костные канальцы; 7 – гаверсовы костные пластинки; 8 – интерстициальные пластинки; 9 – наружные генеральные пластинки.
– формируется путем образования новых слоев на костной поверхности;
– структурной единицей является остеон или гаверсова система – совокупность из 3–25 концентрических костных пластинок. В центре остеона расположен канал, заполненный рыхлой волокнистой соединительной тканью с кровеносными сосудами и нервными волокнами;
– костная пластинка – слой костной ткани толщиной 3–7 мкм;
– коллагеновые волокна в пластинке проходят параллельно друг другу и под углом к волокнам соседних пластинок. Между соседними пластинками в лакунах расположены остеоциты, а в толще пластинки в костных канальцах проходят их отростки;
– каналы Фолькмана связывают каналы остеонов между собой, а также с сосудами и нервами надкостницы;
– снаружи остеон ограничен спайной линией толщиной 1–2 мкм, отделяющей его от фрагментов старых остеонов;
– остеоны ориентированы вдоль длинной оси кости, каналы остеонов расположены параллельно;
– пространства между остеонами заполнены вставочными (интерстициальными) пластинками, которые являются остатками ранее существовавших остеонов, разрушенных в процессе перестройки кости;
– наружные и внутренние общие (генеральные или окружающие) пластинки образуют самый наружный и самый внутренний слои кости под надкостницей и эндостом соответственно.
Периост (надкостница) покрывает снаружи всю кость, за исключением суставной поверхности.
Выделяют два слоя надкостницы – наружный и внутренний:
– наружный (волокнистый) представлен плотной неоформленной волокнистой соединительной тканью, в которой преобладают волокна, идущие параллельно поверхности кости;
– внутренний (остеогенный) состоит из рыхлой волокнистой соединительной ткани, в которой располагаются остеогенные клетки (преостеобласты) и остеобласты;
– пучки прободающих коллагеновых волокон (волокна Шарпея) обеспечивают прочное прикрепление надкостницы к кости;
– надкостница является источником остеогенных клеток для развития, роста и регенерации костной ткани.
Эндост – тонкая оболочка, выстилающая кость со стороны костного мозга. Состоит из тех же слоев, что и периост, но менее выраженных. Содержит остеогенные клетки и остеокласты.
Кровоснабжение кости: кровеносные сосуды, проникающие в надкостницу и эндост, пронизывают матрикс кости через прободающие (фолькмановские) каналы, которые проходят перпендикулярно к гаверсовым, соединяя их между собой.
Гистогенез
Прямой (внутримембранный) остеогистогенез (рис. 6.5, А):
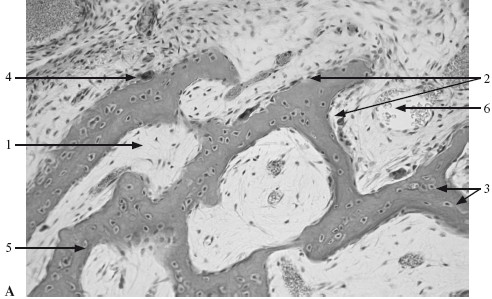
Рис. 6.5. Образование кости.
А – из мезенхимы: 1 – мезенхима; 2 – остеобласты; 3 – остеоциты; 4 – остеокласт; 5 – остеоид; 6 – кровеносные сосуды (×130);
– характерен для развития грубоволокнистой костной ткани;
– этим способом образуются плоские кости черепа, ключицы, дистальные фаланги пальцев;
– мезенхимные клетки группируются в остеогенные островки, которые являются первичными центрами окостенения;
– клетки островков дифференцируются в остеобласты, начинающие вырабатывать остеоид (органический матрикс кости);
– остеоид минерализуется и замуровывает остеобласты, которые превращаются в остеоциты;
– формируются трабекулы, образующие губчатую кость. Непрямой (энхондральный) остеогистогенез (рис. 6.5, Б):
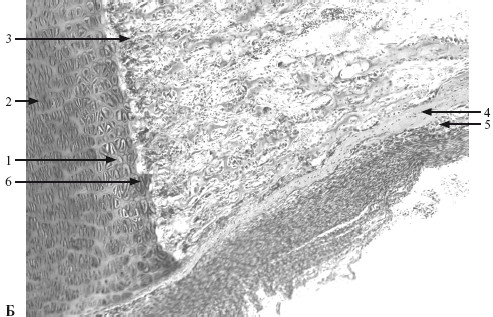
Б – на месте хряща: 1 – зона пузырчатого хряща; 2 – зона столбчатого хряща; 3 – обызвествленный хрящ; 4 – костная манжетка; 5 – надкостница; 6 – костно‑хрящевое соединение (×30).
– из мезенхимы образуются модели трубчатых костей, состоящие из гиалинового хряща;
– первичный центр окостенения (перихондральный) образуется в результате усиленного окостенения надхрящницы и образования в ней грубоволокнистой костной ткани (костная манжетка) в области диафиза;
– в результате этого нарушается питание хряща, возникают дистрофия и дегенерация хондроцитов с образованием в хряще полостей;
– сосуды прорастают из надкостницы в образовавшиеся полости, а вместе с ними остеогенные клетки и остеобласты;
– дифференцировка и продуктивная деятельность их приводит к образованию кости (энхондральное окостенение). На препаратах различимы компоненты комплекса: «кальцинированный хрящ (базофилен) – кальцинированная кость (оксифильна)»;
– костно‑мозговая полость образуется с помощью остеокластов. Образованная ранее костная манжетка растет по направлению к эпифизам, где формируются вторичные центры окостенения;
– хрящевая ткань сохраняется только на суставных поверхностях и в метафизах в виде метаэпифизарной хрящевой пластинки;
– происходит перестройка грубоволокнистой кости в пластинчатую.
Рост трубчатых костей в длину происходит за счет эпифизарной хрящевой пластинки, состоящей из нескольких зон:
– резервная зона покоящегося хряща расположена в эпифизарной части пластинки, состоит из гиалинового хряща, содержащего небольшие хондроциты;
– зона размножения (пролиферативная) состоит из многочисленных делящихся хрящевых клеток, расположенных в виде «монетных» столбиков;
– зона гипертрофии и созревания хряща состоит из крупных вакуолизированных, дегенеративно измененных хондроцитов, прекративших митозы;
– зона кальцификации хряща, где происходят минерализация хрящевого матрикса, гибель хондроцитов и оссификация;
– зона окостенения, где на месте обызвествленного хряща формируется костная ткань.
Перестройка костной ткани:
– кость является динамичной структурой с постоянно изменяющимися формой и внутренней организацией;
– участки кости, испытывающие сжатие, подвергаются резорбции;
– в области приложения тянущих усилий образуется новая костная ткань;
– костные клетки чувствительны к пьезоэлектрическим эффектам, возникающим при деформации кости, что влияет на интенсивность остеогенеза.
Сращение переломов:
– при переломе нарушается кровоснабжение и остеоциты гибнут;
– отмирающая кость подвергается активной резорбции остеокластами;
– между концами отломков формируется костная мозоль вследствие интенсивного размножения остеогенных клеток надкостницы;
– рост сосудов отстает от размножения клеток, поэтому сначала формируется хрящ, который замещается губчатой костью, перестраивающейся затем в компактную. Восстанавливается первоначальная конфигурация кости.
Регуляция роста и регенерации кости:
– паратареоидшый гормон (ПТГ) повышает содержание Са2+ в крови за счет высвобождения его из костей, снижения экскреции его почками и стимуляции перехода витамина D в кальцитриол;
– кальцитонин – антагонист ПТГ, снижает содержание Са2+в крови за счет ингибирования резорбции костей остеокластами;
– активный метаболит витамина D кальцитриол усиливает всасывание Са2+ в желудочно‑кишечном тракте. При дефиците витамина D развивается рахит у детей и остеомаляция у взрослых;
– витамин C необходим для образования коллагена. При его дефиците замедляются рост костей и заживление переломов;
– витамин А поддерживает образование и рост кости. Недостаток его тормозит остеогенез и рост костей, избыток вызывает зарастание эпифизарных хрящевых пластинок и замедление роста кости в длину;
– глюкокортикоиды ухудшают всасывание Са2+ в тонкой кишке;
– при недостатке эстрогенов развивается остеопороз.
Тесты и вопросы для самоконтроля
1. У ребенка, страдающего рахитом, наблюдаются искривление и размягчение костей конечностей. Какой этап костеобразования нарушен?
2. В организме недостаточно витамина С. Какой процесс в развитии костной ткани будет нарушен?
3. Какой патологический процесс будет наблюдаться в костной ткани при избытке паратиреоидного гормона?
4. При рентгеноскопии костей конечностей у больного не обнаружена эпифизарная пластинка роста. Какого возраста достиг больной?
5. С какой особенностью состава костной ткани связана легкость переломов у лиц пожилого возраста и редкость переломов у детей?
Выберите один или несколько правильных ответов:
6. Хондробласты. Верны все утверждения, кроме:
а) располагаются в надхрящнице;
б) участвуют в аппозиционном росте хряща;
в) способны к размножению;
г) участвуют в резорбции хряща.
7. Эластический хрящ. Верны все утверждения, кроме:
а) снаружи покрыт надхрящницей;
б) входит в состав слуховой трубы;
в) с возрастом обызвествляется;
г) содержит эластические и коллагеновые волокна.
8. Какой костной тканью образованы заросшие черепные швы?
а) пластинчатой;
б) компактной;
в) зрелой;
г) грубоволокнистой.
9. Вставочные пластинки в диафизе трубчатых костей – это:
а) материал для образования общих пластин;
б) материал для образования остеонов;
в) оставшиеся части концентрических пластин старых остеонов;
г) часть вновь формирующихся остеонов.
10. Остеобласты:
а) локализуются преимущественно в местах перестройки кости;
б) хорошо развиты гранулярная эндоплазматическая сеть и комплекс Гольджи;
в) характерна невысокая активность щелочной фосфатазы;
г) образуют остеон.
11. Развитие кости на месте хряща:
а) это способ образования плоских костей;
б) костная манжета формируется вокруг эпифиза;
в) сопровождается гипертрофией хондроцитов в центральной части хряща;
г) остеогенные клетки проникают в полости центральной части хряща.
12. Пластинчатая костная ткань. Верно все, кроме:
а) образует компактное и губчатое вещество костей скелета;
б) формируется путем образования новых слоев на поверхности кости;
в) коллагеновые волокна построены из коллагена III типа;
г) коллагеновые волокна в пределах костной пластинки ориентированы упорядоченно;
д) каналы остеонов содержат кровеносные сосуды.
Ответы
1. Минерализация.
2. Образование коллагеновых волокон.
3. Деминерализация костей.
4. 20 лет.
5. С различием в степени минерализации костей.
6 : г.
7 : в.
8 : г.
9 : в.
10 : а, б, г.
11 : б, в, г.
12 : в.
Глава 7
Мышечные ткани
Мышечные ткани (textus musculares) представляют собой группу тканей различного происхождения и строения, объединенных на основании общего признака – выраженной сократительной способности, благодаря которой они могут выполнять свою основную функцию – перемещение тела и его частей в пространстве.
Эти ткани классифицируют по морфологии и функции:
• поперечнополосатая мышечная ткань имеет регулярную поперечнополосатую исчерченность и включает в себя скелетную мускулатуру и сердечную мышцу;
• гладкая мышечная ткань не имеет поперечнополосатой исчерченности и расположена в стенках внутренних органов и кровеносных сосудов;
• сокращение скелетной мускулатуры произвольное (подконтрольно сознанию), в то время как сокращение сердечной и гладкой мускулатуры непроизвольное.
7.1. Поперечнополосатая [скелетная] мышечная ткань
Поперечнополосатая мышечная ткань (textus muscularis striatus [skeletalis]) является самой распространенной мышечной тканью человека. У взрослых мужчин она составляет более 40 % от массы тела, у женщин – 35 %, у детей – около 25 %; при старении ее относительная масса снижается до 28–30 %. Помимо скелетных мышц, обеспечивающих поддержание позы и перемещение тела и его частей в пространстве, она образует глазодвигательные мышцы, мышцы стенки полости рта, языка, глотки, гортани, верхней трети пищевода, наружный сфинктер прямой кишки.
Организация (рис. 7.1):
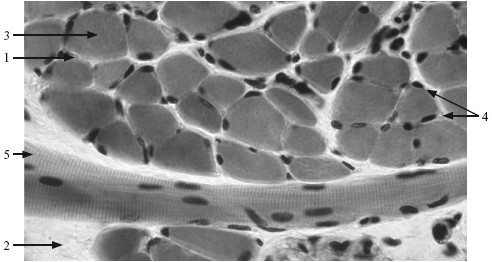
Рис. 7.1. Скелетная мышечная ткань языка. ×400.
1 – эндомизий; 2 – перемизий; 3 – мышечные волокна (срезаны поперечно); 4 – ядра мышечных волокон; 5 – мышечные волокна с поперечной исчерченностью (срезаны продольно).
– состоит из мышечных волокон, окруженных соединительной тканью;
– соединительно‑тканные оболочки связаны с мышцами на трех главных уровнях организации:
– эпимизий окружает всю мышцу;
– перимизий охватывает каждый мышечный пучок, состоящий из 20–100 мышечных волокон;
– эндомизий окружает каждое волокно.
Типы волокон:
– поперечнополосатая мышечная ткань гетерогенна в том смысле, что состоит из трех разных типов волокон;
– типы волокон различаются по содержанию пигмента миоглобина, гликогена, количеству митохондрий и концентрации различных ферментов, способу энергообеспечения. Различают: тип I (красные), тип 11В (белые) и тип IIA (промежуточные).
Красные волокна содержат большое количество пигмента миоглобина, много крупных митохондрий и липидных включений, богаты окислительными ферментами; это тонические, устойчивые к утомлению, с небольшой силой сокращения окислительные волокна;
– характеризуются малым диаметром, относительно тонкими миофибриллами, богатым кровоснабжением;
– получили название «медленные волокна», поскольку легко стимулируются, однако скорость их сокращения низкая, они приспособлены к медленным повторным сокращениям;
– демонстрируют слабое цитохимическое окрашивание на АТФазу;
– энергообеспечение аэробного характера;
– преобладают в мышцах, выполняющих длительные тонические нагрузки (мышцы туловища).
Белые волокна содержат меньше миоглобина и митохондрий, чем красные;
– характеризуются большим диаметром, крупными и сильными миофибриллами, значительным количеством гликогена, сравнительно слабым кровоснабжением;
– бедны ферментами окисления, но богаты фосфорилазами;
– имеют высокую скорость сокращения и приспособлены к быстрым кратковременным усилиям; это тетанические, с большой силой сокращения, легко утомляющиеся гликолитические волокна;
– демонстрируют заметное цитохимическое окрашивание на АТФазу;
– имеют анаэробное энергообеспечение;
– преобладают в мышцах, выполняющих быстрые движения (мышцы конечностей).
Промежуточные волокна обладают характеристиками, промежуточными между уже описанными для красных и белых волокон;
– быстрые, устойчивые к утомлению, с большой силой сокращения окислительно‑гликолитические волокна.
Иннервация определяет дифференцировку типов волокон: красные волокна имеют небольшое количество нервных двигательных окончаний, белые – значительно больше.
Скелетные мышцы человека являются смешанными, т. е. содержат волокна различных типов, которые распределены в них мозаично.
Соотношение красных и белых волокон в мышцах человека индивидуально, предопределено генетически и почти не меняется с возрастом.
Волокна скелетных мыщц – длинные, многоядерные симпласты, образованные миофибриллами. Каждая миофибрилла имеет поперечные полоски (А‑диски и I‑диски), которые повторяются и формируют характерный узор (см. рис. 7.1);
– на гистологических срезах А‑диск анизотропен и обычными гистологическими красителями окрашивается в темный цвет;
– I‑диск изотропен и на обычных гистологических препаратах окрашен светло;
– Z‑линия, или телофрагма, – это плотная область, которая делит I‑диск пополам;
– H‑полоска, или светлая зона, рассекает A‑диск и имеет в центре темную M‑линию, или мезофрагму;
– участок миофибриллы между двумя соседними линиями Z называется миомером, или саркомером, который является структурно‑функциональной единицей поперечнополосатого мышечного волокна;
– в расслабленной мышце длина саркомера составляет около 2–3 мкм, при сокращении мышцы саркомер укорачивается до 1,5 мкм, т. е. почти вдвое;
– на электронной микрофотографии видно, что волокно скелетной мышцы окружено плазматической мембраной, называемой сарколеммой;
– имеет много ядер, лежащих на периферии сразу под сарколеммой;
– цитоплазму мышечного волокна называют саркоплазмой;
– содержит простирающиеся по всей длине волокна миофибриллы;
– миофибриллы имеют вид нитей диаметром 1–2 мкм и длиной, сопоставимой с протяженностью волокна. Их количество в отдельном волокне варьирует в широких пределах – от нескольких десятков до 2000 и более;
– миофибриллы обладают собственной поперечной исчерченностью, причем в мышечном волокне они располагаются так упорядоченно, что А– и I‑диски одних миофибрилл точно совпадают с аналогичными дисками других, обусловливая поперечную исчерченность всего волокна.
Саркоплазматическая сеть – это модифицированная гладкая эндоплазматическая сеть;
– окружает миофиламенты и образует сеть вокруг каждой миофибриллы;
– на границе А– и I‑дисков формирует расширенные терминальные цистерны, которые проходят вокруг миофибрилл;
– цистерны содержат Ca2+;
– регулирует мышечное сокращение путем аккумулирования Ca2+ (ведет к расслаблению) или освобождения Ca2+ (ведет к сокращению миофибрилл).
Триады – характерная черта строения скелетных мышечных волокон:
– будучи расположенной на границе А– и I‑дисков, каждая триада состоит из трубочки (Т‑трубочка) и двух терминальных цистерн саркоплазматической сети;
– Т‑трубочка – это глубокая инвагинация сарколеммы (плазматической мембраны) внутрь мышечного волокна;
– между Т‑трубочкой и терминальными цистернами находятся регулярно расположенные уплотнения (соединительные ножки), представляющие собой зоны низкого электрического сопротивления;
– Т‑трубочки быстро проводят импульсы с наружной поверхности волокна в более глубокие его области, которые запускают механизм выделения Ca2+ из терминальных цистерн в саркоплазму, что способствует сокращению миофиламентов.
Миофибриллы состоят из продольно расположенных цилиндрических пучков белковых нитей – миофиламентов;
– лежат параллельно продольной оси волокна и простираются на всю его длину;
– имеют поперечную исчерченность;
– находятся в определенном положении друг к другу благодаря промежуточным филаментам, состоящим из белков десмина и виментина;
– каждая окружена саркоплазматической сетью. Миофиламенты расположены в миофибрилле строго упорядоченно и подразделяются на тонкие и толстые филаменты;
– I‑диск содержит только тонкие филаменты, которые закрепляются на плотной Z‑линии;
– A‑диск состоит из толстых и тонких филаментов (это обусловливает ее двойное лучепреломление, или анизотропию);
– соотношение тонких и толстых филаментов 6: 1;
– М‑линия образована поперечными соединениями из белка меромиозина между толстыми миофиламентами А‑диска;
– Н‑полоска состоит только из толстых филаментов. Толстые миофиламенты имеют диаметр 10–20 нм и длину 1,5–2,0 мкм;
– состоят из множества молекул фибриллярного белка миозина, организованных так, что они формируют палочковидную структуру (см. рис. 7.1);
– каждая молекула миозина имеет длину 150 нм и толщину 2 нм и выглядит похожей на клюшку для гольфа с двумя головками – глобулярными выступами, имеющими специфический участок для связывания АТФ;
– гидролиз АТФ происходит в головках, которые являются также местом связывания с актином;
– молекула миозина состоит из двух идентичных тяжелых цепочек и двух пар легких цепочек;
– тяжелые цепочки ферментативно расщепляются, формируя два фрагмента – легкий и тяжелый меромиозин;
– легкий меромиозин составляет большую часть палочковидного участка молекулы, в то время как тяжелый меромиозин представляет глобулярную головку и небольшую часть (шейку) палочки;
– молекула миозина может сгибаться, как на шарнирах, в месте соединения тяжелого меромиозина с легким и в области прикрепления головки;
– перемычки, видимые между тонкими и толстыми миофиламентами, сформированы головками молекул миозина плюс небольшая часть палочковидного участка.
Тонкие миофиламенты состоят из F‑актина, который формируется при полимеризации мономеров G‑актина, или глобулярного актина, и двух регуляторных белков – тропонина и тропомиозина;
– имеют в диаметре 5–7 нм и в длину 1 мкм;
– каждый актиновый филамент состоит из двух F‑нитей в форме двойной спирали толщиной 6–7 нм и вариабельной длины;
– нитевидная молекула тропомиозина лежит в углублении актиновой двойной спирали;
– тропонин распределен вдоль тонких филаментов с интервалами 40 нм.
Тропонин – глобулярный белковый комплекс, состоящий из трех субъединиц:
– TnC, которая связывает Ca2+;
– TnT, которая прикрепляется к тропомиозину;
– TnI, которая ингибирует (предотвращает) взаимодействие актина и миозина.
В покое миозиновые головки, с которыми связаны молекулы АТФ, не способны взаимодействовать со специальными (актиновыми) центрами на молекуле актина, так как последние прикрыты комплексом тропонин‑тропомиозин (КТТ).
Сокращение миофибриллы инициируется, когда Ca2+ присоединяются к TnC‑единице тропонина, воздействуя на КТТ;
– возникающее изменение конформации КТТ и смещение молекулы связанного с ним тропомиозина демаскирует (открывает) активные центры на молекуле актина, с которыми связываются миозиновые головки, образуя поперечные мостики;
– одновременно с этим головка молекулы миозина расщепляет АТФ на АДФ с выделением энергии;
– выделенная энергая способствует движению головки миозина и связанные с ней тонкие филаменты;
– таким образом, тонкий филамент скользит вдоль толстого филамента, когда происходит сокращение.
Гипотеза скользящих нитей (гипотеза Хаксли) предполагает, что сами филаменты не изменяют свою длину, а скользят друг вдоль друга, увеличивая степень перекрытия между ними;
– скольжение является результатом повторяющихся соединений и разъединений головок молекул миозина и соседних актиновых филаментов;
– результат: длина саркомера уменьшается практически вдвое;
– тонкие филаменты скользят, проникая глубже в А‑полос‑ку, но сама А‑полоска остается неизменной длины;
– полоска I и полоска H уменьшаются в размере, когда линии Z приближаются к концам полосок A;
– расслабление после мышечного сокращения происходит в результате снижения концентрации Ca2+ в области саркомера, которое вызывает отщепление Ca2+от TnC‑субъединицы тропонина и возвращение тропонина в первоначальное состояние. Нити тропомиозина при этом вновь закрывают активные центры на молекулах актина, что обусловливает прекращение циклического образования мостиков между толстыми и тонкими филаментами.
Опорный аппарат мышечного волокна включает особые элементы цитоскелета (тело– и мезофрагма), а также связанную с ними сарколемму и базальную мембрану.
Телофрагма (линия Z) – область прикрепления тонких миофиламентов двух соседних саркомеров, ее ширина 30–100 нм;
– представляет из себя сложную трехмерную решетку из особых тонких нитей (Z‑филаментов), идущих под углом 45° к оси саркомера и связывающих тонкие миофиламенты друг с другом. В состав линий Z входят также ряд белков: α‑актинин, филамин, Z‑белок.
Мезофрагма (линия M) – плотная линия шириной 75–85 нм, является областью закрепления толстых (миозиновых) филаментов в саркомере. Образована центральными участками миозиновых филаментов, связанных друг с другом мостиками, состоящими из белков миомезина, креатинкиназы и М‑белка.
Титин (коннектин) – белок с эластическими свойствами, нити которого присоединены к толстым филаментам по всей их длине и, продолжаясь в I‑диски, прикрепляют концы толстых филаментов к линиям Z. Нити титина препятствуют перерастяжению мышцы.
Небулин – белок в виде нитей, расположенных по всей ширине I‑диска параллельно тонким филаментам, с которыми он связан, обеспечивая их механическую стабилизацию.
Промежуточные филаменты из белка десмина (толщиной 8– 10 нм) связывают, с одной стороны, соседние телофрагмы одной миофибриллы, с другой – мезофрагмы, а также телофрагмы соседних миофибрилл друг с другом;
– такие же филаменты прикрепляют телофрагмы к сарколемме и элементам системы Т‑трубочек и саркоплазматической сети.
Костамеры – кольца из белка винкулина, охватывающие изнутри мышечное волокно и расположенные перпендикулярно к его длинной оси. Представляют собой участки непосредственного соединения между сарколеммой и подлежащими I‑дисками миофибрилл. Помимо винкулина, в костамерах имеются другие белки, связанные с цитоскелетом: талин, спектрин, α‑актинин.
Энергетический аппарат мышечных волокон представлен митохондриями, располагающимися в виде цепочек под сарколеммой и между миофибриллами, трофическими включениями (гликоген, липиды), которые находятся между миофибриллами по всей толщине миосимпласта, а также миоглобином.
Миоглобин – железосодержащий кислородсвязывающий пигмент мышечного волокна, придающий ему красный цвет. Его способность к связыванию кислорода способствует повышению активности процессов окислительного фосфорилирования, лежащего в основе энергетического обеспечивания мышечного сокращения.
Синтетический аппарат мышечного волокна представлен свободными рибосомами и полирибосомами, цистернами гранулярной эндоплазматической сети и комплексом Гольджи; аппарат внутриклеточного переваривания – лизосомами, необходимыми для постоянно протекающего процесса обновления структурных компонентов мышцы.
Дата добавления: 2019-02-12; просмотров: 192; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
