Определить газовую постоянную смеси
ДОМАШНЕЕ ЗАДАНИЕ ПО ДИСЦИПЛИНЕ ТЕРМОГАЗОДИНАМИКА
Заполнить таблицу «Анализ термодинамических процессов»
| Процесс | Характеристики процесса | |||||||||
| Опред проц | Уравн проц | Граф изобр проц в раб диагр | Связь между парам | Уравн первого закона термод для проц | Измен внутр энергии в проц | Работа в проц | Теплота в проц | Граф изобр проц в тепл диагр | Схемы энерго обмена | |
| Изохорный | ||||||||||
| Изобарный | ||||||||||
| Изотермич | ||||||||||
| Адиабатный | ||||||||||
Решить задачи (10).
2.1. Определить удельный объем углекислого газа, если его масса 2 кг, удельная газовая постоянная 189 Дж /кг*К, при температуре 560С и давлении 4 ат.
2.2. Найти количество теплоты, необходимое для нагревания при постоянном объеме 10 кг азота от 200 до 8000С, если сv =840 Дж/кг*К.
2.3. Дано k и R, найти сv и ср.
2.4. Известно, что для азота ср=1039 Дж/кг*К, определить c'р [Дж/мз* К].
2.5. Баллон с кислородом вместимостью 100 л находится при температуре 200С и манометрическом давлении 10,8 МПа. Давление окружающей среды 100кПа, удельная газовая постоянная 260 Дж/кг*К. Найти массу кислорода.
2.6. Воздух при начальных условиях Т1=850К и V1=0,05м3 при постоянном давлении расширяется до объема V2=0,1 м3. Найти конечную температуру. Как при этих условиях изменится внутренняя энергия воздуха? Сколько теплоты нужно сообщить воздуху для данного изменения объема? Какую работу совершит воздух при расширении? При каком давлении осуществляется данный процесс?
|
|
|
2.7. Воздух с начальным объемом 8 м3 при давлении 90 кПа и температуре 200 изотермически сжимается до давления 0,8 МПа. Найти конечный объем и работу изменения объема.
2.8. Скорость потока в сечении 600 м/с, площадь сечения 0,02 м2, плотность газа 0,8кг/м3. Определить массовый, объемный расходы, плотность потока.
2.9. Во входном устройстве ТРД температура на входе Тн=-300С, скорость потока равна скорости полета Vп=720 км/час, скорость потока на выходе св=135 м/с, ср=1005Дж\кг*К. Определить Тв, Т*н, Т*в.
2.10. При скорости полета Vп=720 км/час, скорость потока на выходе сс=600 м/с, расход воздуха 120 кг/с. Определить Р – тягу двигателя
- Выполнить практические работы, порядок расчета прилагается.
- Оформить задачи и практические работы в тетради (12-18листов) и сдать на проверку. На титульном листе тетради указать название дисциплины, шифр группы, ФИО преподавателя и студента, выполнявшего работу. Таблицу оформить на отдельном листе и вложить в тетрадь.
ПРАКТИЧЕСКАЯ РАБОТА № 1
ОПРЕДЕЛЕНИЕ ТЕРМОДИНАМИЧЕСКИХ ПАРАМЕТРОВ ГАЗОВОЙ СМЕСИ
Цель работы: определить термодинамические параметры газовой смеси по индивидуальным исходным данным.
|
|
|
Исходные данные
| Вариант | CO2 % | H2 % | N2 % | H2O % | SO2 % | CO % | O2 % | p см кгс/см2 | v см м3 | t см °С |
| 1 | 12 | — | 75 | 8 | —— | 5 | — | 0,95 | 2 | 2000 |
| 2 | 10 | — | 80 | — - | —— | 8 | 2 | 1,00 | 3 | 450 |
| 3 | — | 5 | 70 | 10 | —— | — | 15 | 0,90 | 4 | 500 |
| 4 | 13 | — | 75 | 6 | —— | 6 | — | 1,05 | 5 | 150 |
| 5 | — | 10 | 50 | 10 | —— | — | 30 | 1,05 | 6 | 200 |
| 6 | 5 | 30 | 55 | — | —— | — | 10 | 0,85 | 7 | 350 |
| 7 | 14 | — | 77 | 5 | —— | 4 | — | 0,70 | 8 | 400 |
| 8 | — | 5 | 75 | — | —— | — | 20 | 0,95 | 9 | 100 |
| 9 | — | — | 60 | 15 | 10 | 15 | — | 1,00 | 10 | 300 |
| 10 | 15 | — | 76 | 4 | — | 5 | — | 1,05 | 2 | 600 |
| 11 | 20 | — | — | 15 | — | 55 | 10 | 1,15 | 3 | 700 |
| 12 | 16 | — | 76 | 4 | — | 4 | 10 | 1,20 | 4 | 750 |
| 13 | 8 | 5 | 85 | — | — | — | 2 | 1,25 | 5 | 700 |
| 14 | 15 | — | 75 | 5 | — | 5 | — | 1,05 | 6 | 800 |
| 15 | — | 20 | 50 | — | — | 20 | 10 | 0,85 | 7 | 1000 |
| 16 | 18 | — | 65 | — | 16 | — | 1 | 1,20 | 8 | 1200 |
| 17 | — | 15 | 45 | 15 | — | 25 | — | 1,00 | 9 | 1000 |
| 18 | 14 | — | 76 | 6 | — | 4 | — | 0,90 | 10 | 2000 |
| 19 | — | 2 | 65 | — | 8 | — | 25 | 1,00 | 2 | 450 |
| 20 | — | 10 | 70 | — | 15 | 5 | — | 1,05 | 3 | 350 |
| 21 | 10 | — | 75 | 5 | — | 10 | — | 1,05 | 4 | 600 |
| 22 | — | 5 | 80 | — | — | 5 | 10 | 1,00 | 5 | 550 |
| 23 | 17 | — | 74 | 5 | — | 4 | — | 0,95 | 6 | 400 |
| 24 | 10 | 10 | 60 | — | — | — | 20 | 1,15 | 7 | 1000 |
| 25 | — | 2 | 55 | — | 15 | — | 28 | 0,85 | 8 | 1000 |
| 26 | — | 8 | 62 | — | 15 | — | 15 | 0,95 | 3 | 1000 |
| 27 | — | 16 | 15 | — | 30 | 4 | 35 | 1,2 | 9 | 800 |
| 28 | 10 | — | 80 | 5 | — | 5 | — | 1,0 | 4 | 600 |
| 29 | 28 | 2 | 55 | — | 15 | — | — | 0,8 | 7 | 1000 |
| 30 | — | 10 | 54 | 6 | — | 10 | 20 | 0,9 | 5 | 900 |
| 31 | 12 | 28 | 13 | 27 | — | 20 | — | 1,05 | 3 | 700 |
| 32 | 5 | 10 | 35 | 45 | — | 55 | — | 0,85 | 6 | 1000 |
Содержание работы
|
|
|
|
|
|
1. Выразить исходные данные в единицах системы СИ.
Определить состав смеси в массовых долях.
Так как содержание компонентов смеси задано в процентах, то для определения массовой доли достаточно значение, указанное в таблице, разделить на 100%. Например: CO2 =12%, следовательно, g CO 2 = 0,12
Провести расчет параметров газовой смеси.
Определить молярную массу компонентов.
Молярная масса компонента определяется с помощью таблицы «Периодическая система элементов Д.Ф. Менделеева». По атомной массе компонента определяем молекулярную массу и соответственно молярную.
Например: атомная масса кислорода, примерно, равна 16, а молекулярная 32, т.к. в молекуле кислорода два атома. Соответственно молярная масса кислорода будет составлять µО2 = 32 кг/кмоль, молекулярная масса СО2 = 12+ (16*2) = 44, следовательно µсО2 =44 кг/кмоль.
3.2. Определить газовые постоянные компонентов смеси
Ri = 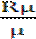
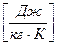
 ,
,
где Ri 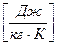 - удельная газовая постоянная компонента смеси, Rµ =8314
- удельная газовая постоянная компонента смеси, Rµ =8314 
Определить газовую постоянную смеси
Rcм = 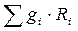
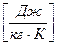 , где gi - массовая доля компонента
, где gi - массовая доля компонента
Дата добавления: 2019-01-14; просмотров: 654; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
