Мембраны и мембранные процессы
Полупроницаемые перегородки, при помощи которых осуществляется осмос (см. рис. 9.4), называют мембранами. Мембраны — это тонкие пористые пленки, пронизанные мельчайшими каналами, размер которых обычно не превышает 10 нм. По этой причине мембраны относятся к двухмерным высокодисперсным системам.
Для изготовления мембран, которые используют в технике, применяют керамику и некоторые другие материалы; чаще все же — синтетические полимеры.
Кроме осмоса (см. параграф 9.4) при помощи мембран можно осуществлять ряд других процессов — их называют мембранными. Они основаны на преимущественной проницаемости растворителя, одного или нескольких компонентов жидкой или газовой среды через разделительную перегородку — мембрану (рис. 12.6).

Рис. 12.6. Характеристика мембранных процессов (а – размер пор)
Разностороннее применение мембран в технике заимствовано у живой природы. Клетки растительных и животных организмов являются микроскопическими образованиями; размеры их чаще всего составляют 10—100 мкм. Снаружи клетки ограничены мембраной, толщина которой не превышает 10 нм, т.е. в тысячи раз меньше размерена самой клетки. Специфическое неоднородное строение мембран позволяет регулировать обмен веществ: впускать в клетку необходимые для жизнедеятельности вещества (аминокислоты, сахара, жирные кислоты, некоторые ионы и др.) и выпускать из клетки подлежащие удалению вещества, обеспечивая тем самым внутриклеточный обмен за счет избирательной проницаемости мембран.
Одним из важнейших направлений применения мембранных процессов является получение жидкости без примесей (молекул, ионов) при помощи обратного осмоса. Для его осуществления используют мембраны с размерами пор менее 1 нм. Подобные мембраны, которые можно изготовить из ацетата целлюлозы, обладают особыми свойствами: они способны задерживать растворенные в жидкости молекулы и даже ионы.
В отличие от рис. 9.4 на рис. 12.7, а приведена схема другого варианта осмоса, особенности которого были рассмотрены в параграфе 9.4. Если со стороны дисперсной системы или раствора 2 приложить давление р, превышающее осмотическое, то поток жидкости (растворителя) из области 2 будет перемещаться в область 1. Через мембрану 3 проходят только молекулы растворителя (вследствие их большей подвижности).
Частицы, крупные молекулы и ионы растворенного вещества останутся в области 2. Таким образом содержимое области 1 будет обогащаться чистой жидкостью, а в области 2 увеличится концентрация частиц дисперсной фазы или растворенного вещества.
Направление движения жидкости 4 при обратном осмосе (см. рис. 12.7, б) противоположно направлению ее движения в случае осмоса (см. рис. 11.7, а). По этой причине движение жидкости через мембрану под действием внешнего давления и получило название «обратный осмос».
Работа, необходимая для осуществления обратного осмоса Wос, в основном расходуется на продавливание жидкости через поры полупроницаемой перегородки. Эту работу можно представить в виде
Wос = ΔpV, (12.12)
где Δp — перепад давления по обе стороны мембраны; V — объем жидкости, прошедшей через поры мембраны.
В свою очередь величина Δр имеет вид
Δp = p – π, (12.13)
где p — избыточное давление над раствором; π — осмотическое давление, которое определяется по формуле (9.13).

Рис. 12.7. Схема осмоса ( а ), обратного осмоса ( б ), диализа и ультрафильтрации ( в ):
1 — дисперсионная среда (чистая жидкость); 2 — коллоидный или истинный раствор; 3 — мембрана (полупроницаемая перегородка);
4 — поток чистой жидкости (растворителя); 5 — поток примесей
Из равенства (12.13) следует, что
р > π. (12.14)
Условие (12.14) определяет избыточное давление, необходимое для осуществления обратного осмоса. Значение этого давления зависит от осмотического давления, которое для некоторых растворов приведено в параграфе 9.4.
Обратный осмос можно использовать, например, для опреснения морской воды. Осмотическое давление морской воды, содержащей 3,5% растворенных солей, составляет 25∙105 Па, или примерно 25 атм. Для осуществления обратного осмоса в процессе опреснения морской воды внешнее давление Р должно превышать 25 атм. Морская вода помещается в сосуд 2, в котором в дальнейшем концентрируются примеси (см. рис. 12.7, б), задерживаемые мембраной. Чистая вода проходит через мембрану и собирается в полости 1.
Возможности мембранных процессов не исчерпываются обратным осмосом. Так, при помощи диализа, схема которого приведена на рис. 12.7, в происходит очистка дисперсной системы (коллоидного раствора) или раствора ВМС от содержащихся в них примесей в виде ионов или молекул. Очистка обеспечивает устойчивость дисперсных систем. Коллоидный раствор или раствор ВМС помещают в правую часть 2 сосуда, отделенную от левой части 1 мембраной 3. Мембрана проницаема для молекул и ионов, но задерживает частицы дисперсной фазы и макромолекулы ВМС. Примеси в результате диффузии из области большей концентрации (правая часть сосуда) самопроизвольно будут переходить в область меньшей концентрации (левая часть сосуда); поток примесей на рис. 12.7, в показан стрелками 5. Если периодически менять внешний раствор 1, то процесс диффузии и очистки можно ускорить. В результате в области 1 будут собираться примеси, которые ранее находились в области 2, а коллоидный раствор или раствор ВМС очистится от них.
Интенсифицировать очистку коллоидного раствора при помощи диализа можно путем приложения внешнего давления р (см. рис. 12.7, в). В этом случае процесс называют ультрафильтраицией.
Некоторые важные функции почек человека (выделение отработанных продуктов из крови, регулирование кровяного давления, а также водного и электролитного баланса) достаточно полно воспроизводит искусственная почка, которая работает по принципу диализа и ультрафильтрации. В искусственной почке вследствие диализа и ультрафильтрации происходит удаление из плазмы крови ядовитых продуктов (мочевины, мочевой кислоты, токсинов и др.).
Обратный осмос, диализ и ультрафильтрация хотя и применяются для различных целей (см. рис. 12.7), но имеют много общего: используются аналогичная аппаратура и внешнее давление (за исключением диализа). Особенности этих процессов заключаются в механизме и в размере пор. Обратный осмос (см. рис. 12.7, б) в отличие от диализа и ультрафильтрации служит для концентрирования истинных и коллоидных растворов и извлечения растворителя. При обратном осмосе из раствора через полупроницаемую перегородку движется чистый растворитель. По этой причине размер пор мембран должен быть небольшим, менее 1 нм, чтобы через них могли проходить молекулы растворителя и задерживаться молекулы примесей.
При диализе и ультрафильтрации (см. рис. 12.7, в) очистки от примесей подвергается коллоидный раствор (высокодисперсные системы типа Т/Ж и Ж/Ж) или раствор ВМС. Через полупроницаемую перегородку движутся примеси, которые находятся в растворенном виде. Размеры частиц дисперсной фазы коллоидных растворов и макромолекул относительно большие. По этой причине поры мембраны должны пропускать примеси и задерживать коллоидные частицы и макромолекулы ВМС. В связи с этим для осуществления диализа и ультрафильтрации размер пор должен быть в пределах от 1 до 10 нм, т.е. большим, чем в случае обратного осмоса.
Таким образом, основной принцип действия мембран заключается в избирательной проницаемости, которая определяется размерами пор мембран, свойствами очищаемых систем и внешним давлением.
Эффективность мембранных процессов разделения оценивается следующими показателями:
— селективностью  (l2.14, a)
(l2.14, a)
 где с1 и с2 — концентрация компонентов исходной смеси и прошедших через мембрану:
где с1 и с2 — концентрация компонентов исходной смеси и прошедших через мембрану:
— коэффициентом разделения

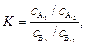 (12.14, б)
(12.14, б)
где сА.1, сВ1 и сА.2, сВ.2 — концентрация компонентов А и В в исходной смеси и прошедших через мембрану;
— проницаемостью, или удельной производительностью
 (12.14, в)
(12.14, в)
где V — объем смеси, прошедшей через мембрану за время τ; В — площадь поверхности мембраны.
В процессе обычной фильтрации продукт в виде осадка закрепляется на поверхности фильтра, что приводит к необходимости его периодической регенерации. При использовании мембран раствор и примеси проходят через поровое пространство, а возможность создания избыточного давления в случае обратного осмоса и особенно при ультрафильтрации позволяет избежать или, во всяком случае, резко сократить накопление примесей на поверхности мембран и тем самым исключить необходимость их частой очистки.
Для интенсификации процесса очистки с помощью мембран применяют электродиализ, схема которого дана на рис. 12.8. Коллоидный раствор или раствор ВМС 1 помещают между двумя полупроницаемыми перегородками 2, пропускающими ионы дисперсионной среды. В корпус вмонтированы электроды 3. Совместным воздействием электрического поля и внешнего давления обеспечивают более полное удаление примесей из жидкой дисперсионной среды.
Кроме очистки растворов, мембраны способствуют равновесию электролитов в присутствии частиц или ионов, размеры которых не позволяют им проникать через поры этих перегородок; возникает так называемое мембранное равновесие.
Схема мембранного равновесия показана на риc. 12.9. По обе стороны полупроницаемой перегородки 1 могут находиться два раствора с концентрациями с1 и с2 причем с2 > с1. Перегородка способна пропускать ионы Na+ и Сl– и непроницаема для катионов Кz+, размеры которых соответствуют высокодисперсным системам. Концентрация ионов Na+ и Сl– в растворе, находящемся справа от перегородки, больше, чем в растворе слева. Поэтому часть ионов Na+ и Сl– (см. рис. 12.9, а) пройдет через мембрану из области большей концентрации в область меньшей концентрации, т.е. справа налево. В условиях равновесия (см. рис. 12.9, б) концентрация ионов Na+ и Сl– справа от мембраны уменьшится на х, слева от мембраны концентрация ионов Кz+ останется неизменной, а концентрация ионов Сl– возрастет на х, и появятся ионы Na+ с концентрацией х.
|
|
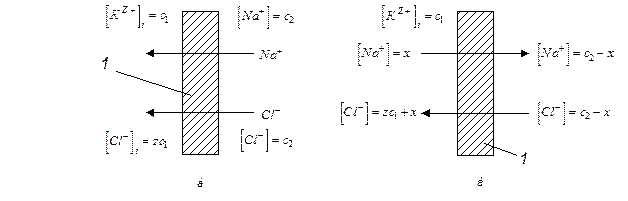
Рис.12.9. Схема мембранного paвновесия Доннана:
a — начальное положение; б — после установления равновесия:
1 — мембрана, полупроницаемая перегородка
Изменение концентрации ионов Na+ и Сl–, на величину х и можно определить из условий, когда произведение концентраций диффундирующих ионов в обоих растворах одинаково, т.е.
 (12.15)
(12.15)
откуда определится величина х:
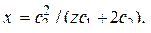 (12.16)
(12.16)
Доля электролита NaCl x/c2 составляет
 (12.17)
(12.17)
Для анализа уравнений (12.16) и (12.17) следует рассмотреть два крайних случая. Первый из них, когда концентрация электролита значительно превышает концентрацию коллоидного раствора, т.е. с2 >> с1 и величиной с1 можно пренебречь. В этих условиях из уравнения (12.17) следует
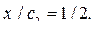 (12.18)
(12.18)
Условие (12.18) означает, что электролит (NaCl) распределяется поровну по обе стороны мембраны.
Когда концентрация электролита незначительна, т.е. с2 << с1, то
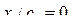 (12.19)
(12.19)
Согласно условию (12.19) электролит практически остается в исходном положении, и мембранное равновесие не проявляется.
Условия (12.18) и (12.19) подтверждаются экспериментально: так, при с2/c1 = 100 NaCl практически поровну (49 и 51% соответственно) распределяется между растворами. Когда с2/с1 = 0,01, то подавляющее большинство электролита (99%) остается в правой части.
Мембранное равновесие, которое по имени первого исследователя называют равновесием Доннана, имеет практическое значение для растворов ВМС, при набухании веществ и в различных физиологических процессах.
Дата добавления: 2018-11-24; просмотров: 368; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
