Применение 1-ого закона термодинамики к изопроцессам.
Основы термодинамики
ВНУТРЕННЯЯ ЭНЕРГИЯ
Под внутренней энергией термодинамической системы понимают кинетическую энергию теплового движения ее молекул и потенциальную энергию их взаимодействия. Она зависит от параметров состояния V,T . Внутренняя энергия идеального одноатомного газа прямо пропорциональна его абсолютной температуре:
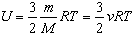
Для газов, состоящих из более сложных молекул, также U ~ Т , но коэффициент пропорциональности другой. Это объясняется тем, что такие молекулы не только движутся поступательно, но и вращаются.
РАБОТА В ТЕРМОДИНАМИКЕ
Если газ расширяется при постоянном давлении р, то сила, действующая со стороны газа на поршень: F = рS, гдеS - площадь поршня.
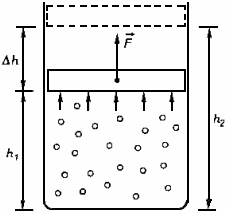
При подъеме поршня на высоту 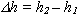 газ совершает работу
газ совершает работу
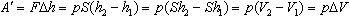
где ΔV - изменение объема газа.
При медленном сжимании газа работа, совершаемая внешними телами над газом, будет отличаться только знаком:

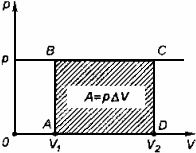
Работа, совершаемая термодинамической системой при постоянном давлении, равна
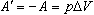
КОЛИЧЕСТВО ТЕПЛОТЫ
Процесс передачи энергии от одного тела к другому без совершения работы называют теплообменом.
Количество теплоты - это энергия, переданная телу в результате теплообмена.
Теплоемкость С - количество теплоты, необходимое для нагревания тела массой m на 1 К. Удельная теплоемкость с - это количество теплоты, которое получает или отдает 1 кг вещества при изменении его температуры на 1 К: c=C/m
|
|
|
Для изменения температуры вещества массой m от Т1 до Т2 ему необходимо сообщить количество теплоты
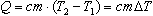
Коэффициент с в этой формуле называют удельной теплоемкостью: [с]=1 Дж/(кг*К).
При нагревании тела Q > 0, при охлаждении Q < 0.
Для того, чтобы жидкость массы m полностью превратить в пар, ей необходимо передать количество теплоты
Q=rm
где r - удельная теплота парообразования: [r] = 1 Дж/кг .
Удельная теплота парообразования - это количество теплоты, которое необходимо для превращения 1 кг жидкости в пар при постоянной температуре.
Конденсация - процесс, обратный испарению.
Для того, чтобы расплавить полностью тело массой m , ему необходимо сообщить количество теплоты
Q= λm
где - удельная теплота плавления: {λ} = 1 Дж/кг .
Удельная теплота плавления - это количество теплоты, которое необходимо для плавления 1 кг кристаллического вещества при температуре плавления.
Кристаллизация - процесс, обратный плавлению.
Для замкнутой системы, состоящей из N тел, можно записать уравнение теплового баланса:
Q1+...+Qn=0
где Q1, ... , QN - количества теплоты, полученные или отданные телами.
ПЕРВЫЙ ЗАКОН ТЕРМОДИНАМИКИ
Закон сохранения энергии
|
|
|
Энергия не возникает из ничего и не исчезает, она только переходит из одной формы в другую. Закон сохранения энергии, распространенный на тепловые явления, называется первым законом термодинамики.
Первый закон термодинамики
Изменение внутренней энергии системы при переходе из одного состояния в другое равно сумме работы внешних сил и количества теплоты, переданного системе:
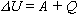
Этот закон можно сформулировать иначе:
Количество теплоты, переданное системе, идет на изменение ее внутренней энергии и на совершение системой работы над внешними телами:
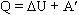
В первой формулировке А - работа, совершаемая над системой (над газом), во второй А' - это работа, совершаемая системой (газом).
Вечный двигатель первого рода - устройство, способное совершать неограниченное количество работы без подведения энергии извне.
Из первого закона термодинамики следует невозможность создания вечного двигателя первого рода. Если к системе не поступает теплота, то
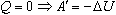
Иными словами, работа совершается системой за счет уменьшения ее внутренней энергии. После того, как запас энергии будет исчерпан, двигатель перестанет работать.
Процесс, протекающий в теплоизолированной системе, называют адиабатным.
|
|
|
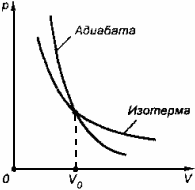
Абсолютно исключить теплопередачу невозможно, но иногда реальные процессы близки к адиабатным. Они протекают за очень малый промежуток времени, в течение которого не происходит существенного теплообмена между системой и внешними телами.
Применение 1-ого закона термодинамики к изопроцессам.
| ПРИМЕНЕНИЕ 1 ЗАКОНА ТЕРМОДИНАМИКИ К ИЗОПРОЦЕССАМ. | |||||
| Процесс | Постоянные | График | Изменение внутренней энергии | Запись 1-го закона термодинамики | Физический смысл |
| Изотермическое расширение | m=const M=const T=const pV=const | 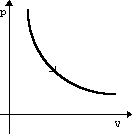
| U=const ΔU=0 | Q=A' | Изотермический процесс не может происходить без теплопередачи. Все количество теплоты, переданное системе, расходуется на совершение этой системой механической работы. |
| Изотермическое сжатие | m=const M=const T=const pV=const | 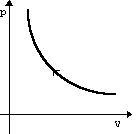
| U=const ΔU=0 | A=-Q | Изотермический процесс не может происходить без теплопередачи. Вся работа внешних сил выделяется в виде тепла. |
| Изохорное нагревание | m=const
M=const
V=const 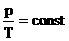
| 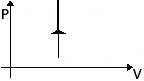
| p↑ T↑ U↑ ΔU>0 | A=0 Q= ΔU | Все количество теплоты, переданное системе, расходуется на увеличение ее внутренней энергии. |
| Изохорное охлаждение | m=const
M=const
V=const 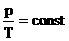
| 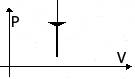
| p↓ T↓ U↓ ΔU<0 | A=0 Q= ΔU<0 | Система уменьшает свою внутреннюю энергию, отдаваятепло окружающим телам. |
| Изобарное расширение (нагревание) | m=const
M=const
p=const
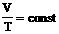
|

| V↑ T↑ U↑ ΔU>0 | Q=ΔU+A' ΔU=Q-А'>0 | Количество теплоты, переданное системе, превышает совершенную еюмеханическую работу. Часть тепла расходуется на совершение работы, а часть – на увеличениевнутр. энергии. |
| Изобарное сжатие (охлаждение) | m=const
M=const
p=const
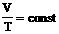
| 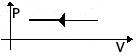
| V↓ T↓ U↓ ΔU<0 | ΔU=Q+A<0 Q<0 | Количество теплоты, отдаваемое системой, превышает работу внешних сил. Часть тепла система отдает за счет уменьшениявнутр. энергии. |
| Адиабатное Расширение | m=const
M=const
 =const =const
| 
| ΔU<0 U↓ T↓ | Q=0 A' > 0 Δ U=-A' < 0 A'=- Δ U | Система совершает механическую работу только за счет уменьшения своей внутренней энергии. |
| Адиабатное сжатие | m=const
M=const
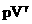 =const =const
| 
| ΔU>0 U↑ T↑ | Q=0 A>0 ΔU=A | Внутренняя энергия системы увеличивается за счет работы внешних сил. |
|
|
|
ТЕПЛОВЫЕ ДВИГАТЕЛИ
Тепловые двигатели - устройства, превращающие внутреннюю энергию топлива в механическую энергию.
Любой тепловой двигатель состоит из трех основных частей.
Рабочее тело - газ, совершающий работу А' при расширении.
Нагреватель - устройство, от которого рабочее тело получает количество теплоты Q 1
Холодильник - устройство, которому рабочее тело передает количество теплоты Q2
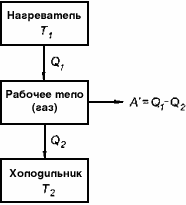
Коэффициентом полезного действия (КПД) теплового двигателя называют отношение работы,совершаемой двигателем, к количеству теплоты, полученному от нагревателя:

Так как Q2 < Q1, то 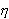 всегда < 1.
всегда < 1.
Идеальная тепловая машина Карно - модель теплового двигателя, в котором рабочим телом является идеальный газ. КПД машины Карно
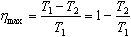
где Т1 - температура нагревателя, T2 - температура холодильника.
Реальная тепловая машина не может иметь КПД, превышающий КПД идеальной тепловой машины.
Пример. Объем кислорода массой 160 г, температура которого 27°С, при изобарном нагревании увеличился вдвое. Найдите работу газа при расширении, количество теплоты, которое пошло на нагревание кислорода, изменение внутренней энергии.
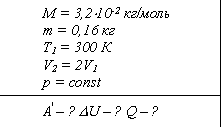
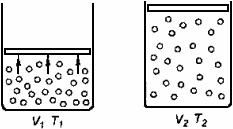
Величина работы, совершаемой газом при изобарном процессе, когда V = V2 - V1 = V1, определяется выражением

С учетом уравнения состояния

можно записать
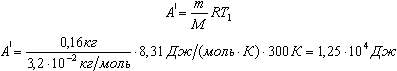
Изменение внутренней энергии двухатомного газа, с учетом уравнения состояния, будет выглядеть:
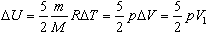
Учитывая, что А| = pV1, получим: 
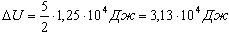
Количество теплоты, переданное газу, согласно первому закону термодинамики, идет на изменение его внутренней энергии и совершение газом работы:
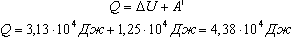
Ответ: работа газа равна 12,5 кДж, количество теплоты, которое пошло на его нагревание, равно 43,8 кДж, изменение внутренней энергии - 31,3 кДж .
Дата добавления: 2018-11-24; просмотров: 201; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
